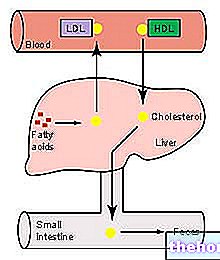
Táto metabolická cesta zahŕňa niekoľko fáz: cholesterol sa prenáša z periférnych tkanív do pečene najskôr lymfatickým systémom, potom krvným obehom. Hlavnými zložkami, ktoré sa zúčastňujú reverzného transportu cholesterolu, sú HDL, ABCA1 a apo A-I.
nečrevné alebo pečeňové, periférne bunky nie sú schopné degradovať prebytočný cholesterol; preto, aby sa zachovala bunková homeostáza, je nevyhnutná prítomnosť mechanizmu určeného na odstraňovanie cholesterolu.
Tento mechanizmus zameraný na obnovu prebytočného periférneho cholesterolu v pečeni sa nazýva „reverzný transport cholesterolu“ (RCT: reverzný transport cholesterolu).
(fosfolipidy a cholesterol), čo vedie k zostaveniu a tvorbe zrelých častíc HDL.Predchodcovia HDL
Prvá etapa reverzného transportu cholesterolu spočíva v produkcii diskoidných prekurzorov HDL v čreve a pečeni, ktoré vystavujú na svojom povrchu apoproteíny (hlavne ApoA-I).
Uvoľňujú sa teda prekurzorové molekuly HDL nazývané pre-B-HDL, ktoré obsahujú veľmi malé množstvo cholesterolu a lipidov, najmä fosfolipidov.Prítomnosť týchto prekurzorových molekúl na periférnej úrovni podporuje prenos prebytočného voľného cholesterolu (FC) - uniknutého z buniek periférneho tkaniva - do apo AI prostredníctvom zásahu membránového transportéra nazývaného kazeta A1 viažuca ATP (ABCA1).
Tento transportér je lokalizovaný na povrchu bunky a v Golgiho membránach a môže transportovať lipidy z Golgiho aparátu do bunkovej membrány, čím uľahčuje ich odtok.
V tomto mieste, akonáhle voľný cholesterol vstupuje do natívneho HDL, zasiahne plazmatický enzým pečeňového pôvodu, nazývaný plazmatický lecitín-cholesterolester acyltransferázy alebo jednoduchšie LCAT; tento enzým premieňa voľný cholesterol zabudovaný v pre-B-HDL na estery cholesterolu, pričom transformuje pre-B-HDL do svojej zrelej a-HDL formy; v praxi nepretržitá akumulácia cholesterolu v lipoproteínovom jadre prevádza diskoidálne HDL na sférické a kypré častice, ktoré môžu ďalej získavať apoproteíny z lipoproteínových častíc bohatých na triglyceridy a navzájom sa spájať.
V celom procese zohráva kľúčovú úlohu apolipoproteín AI, ktorý stimuluje aktivitu transportéra ABCA1 a LCAT. Pretože ApoAI je v HDL najviac zastúpeným apolipoproteínom, jeho plazmatická koncentrácia priamo súvisí s hladinami HDL cholesterolu.
UPOZORNENIE: esterifikačný proces je zásadný pre zabránenie opätovnej difúzie cholesterolu z HDL do plazmatickej membrány; tento mechanizmus využíva mastnú kyselinu v polohe dva prítomnej v molekulách fosfatidylcholínu.
LCAT-sprostredkovaná esterifikačná metóda potom transformuje molekuly pre-B-HDL do ich "zrelého" sférického tvaru a-HDL. Tieto lipoproteíny sú potom transportované do pečene, kde uvoľňujú cholesterol, dvoma rôznymi cestami.
Prvá pečeňová cesta
V prvom prípade HDL bohatý na esterifikovaný cholesterol prenáša tento lipid na lipoproteíny bohaté na triglyceridy (lipoproteíny s veľmi nízkou a nízkou hustotou), ktoré sú potom zachytené v pečeni prostredníctvom špecifických receptorov (LDL-R) a odstránené z obehu.
Cieľom je dopraviť periférny cholesterol do pečene prostredníctvom receptorového systému LDL, potom "vypustiť" HDL z prebytočného cholesterolu na periférnej úrovni, aby bol opäť dostupný pre jeho prijatie z tkanív; Vyčerpaním cholesterolu HDL prijímajú výmenou triglyceridy a to sa deje vďaka proteínu na prenos esteru cholesterolu (CETP).
Úlohou tohto proteínu je teda uprednostniť redistribúciu a rovnováhu esterov cholesterolu a triglyceridov medzi lipoproteínmi HDL, LDL, IDL, VLDL, chylomikrónmi a zvyškami chylomikrónov, čo vedie, ako čistý výsledok, k obohateniu triglyceridov o HDL, na úkor esterov cholesterolu a zníženie veľkosti HDL.
Druhá cesta pečene
Druhá cesta zahŕňa pečeňové receptory SR-B1 pre HDL bohaté na esterifikovaný cholesterol v neprítomnosti súčasnej degradácie proteínovej časti HDL, ktorá sa potom recykluje. V praxi tento enzým umožňuje HDL vyprázdniť ich obsah a regenerovať nové pre-B-HDL.
Časť HDL a ApoA-I je však internalizovaná a degradovaná na lyzozomálnej úrovni, a to v pečeňových aj obličkových bunkách. Príjem sprostredkovaný SR-B1 je účinnejší pomocou aktivity pečeňovej lipázy, schopnej remodelovať HDL hydrolyzáciou povrchových fosfolipidov a umožnením toku esterifikovaného cholesterolu z lipoproteínového jadra smerom k plazmatickej membráne (predpokladá sa, že medzi „inými , že ApoE sa tiež podieľa na selektívnom vychytávaní, pretože myši s nedostatkom génu ApoE vykazujú zníženie účinnosti tejto dráhy.) SR-BI je exprimovaný hlavne v pečeni, nadobličkách a vaječníkoch.






.jpg)