Účinné látky: erytropoetín (epoetín alfa)
EPREX 2 000 IU / ml, 4 000 IU / ml, 10 000 IU / ml a 40 000 IU / ml ROZTOK NA INJEKCIE vo vopred naplnených injekčných striekačkách
Prečo sa používa Eprex? Načo to je?
Čo je EPREX a na čo slúži?
EPREX obsahuje účinnú látku epoetín alfa, proteín, ktorý stimuluje kostnú dreň, aby produkovala viac červených krviniek, buniek, ktoré nesú hemoglobín (látka schopná prenášať kyslík). Epoetín alfa je kópiou ľudského erytropoetínu a účinkuje v ňom.
- EPREX sa používa na liečbu symptomatickej anémie spôsobenej zlyhaním obličiek.
- u detí na hemodialýze
- u dospelých na hemodialýze a peritoneálnej dialýze
- u dospelých s ťažkou anémiou, ktorí ešte nepodstupujú dialýzu.
Ak máte zlyhanie obličiek a vaše obličky neprodukujú dostatok erytropoetínu (ktorý je potrebný na tvorbu červených krviniek), môžete mať v krvi málo červených krviniek. EPREX je predpísaný na stimuláciu kostnej drene, aby produkovala viac červených krviniek.
- EPREX sa používa na liečbu anémie, ktorá môže vzniknúť počas chemoterapie solídnych nádorov, malígneho lymfómu alebo mnohopočetného myelómu (rakovina kostnej drene), ak si váš lekár myslí, že budete potrebovať transfúziu krvi. EPREX môže znížiť potrebu transfúzií.
- EPREX sa používa na liečbu stredne anemických pacientov, ktorí majú záujem uložiť svoju krv v očakávaní chirurgického zákroku, aby ju bolo možné transfúzovať počas operácie alebo po nej. Keďže EPREX stimuluje tvorbu červených krviniek, je možné týmto ľuďom odobrať krv. väčšie množstvo krvi.
- EPREX sa používa na liečbu stredne anemických dospelých pacientov, ktorí podstupujú veľký ortopedický chirurgický zákrok (napr. Náhrada bedrového alebo kolenného kĺbu), aby sa znížila potreba krvných transfúzií.
Kontraindikácie Kedy by sa Eprex nemal používať
Nepoužívajte EPREX
- Ak ste alergický (precitlivený) na epoetín alfa alebo na ktorúkoľvek z ďalších zložiek EPREXU (uvedené v časti Obsah balenia a ďalšie informácie);
- Ak vám bola diagnostikovaná „čistá aplázia červených krviniek (kostná dreň nemôže vytvárať dostatok červených krviniek) po predchádzajúcej liečbe ktoroukoľvek látkou, ktorá stimuluje tvorbu červených krviniek (vrátane EPREXU). Pozri časť Možné vedľajšie účinky.
- Ak máte problémy s nekontrolovaným vysokým krvným tlakom
- Stimulovať tvorbu červených krviniek (aby z vás bolo možné odobrať viac krvi), ak nemôžete dostať transfúziu vlastnej krvi počas alebo po chirurgickom zákroku.
- Ak máte podstúpiť elektívny veľký ortopedický chirurgický zákrok (napr. Náhradu bedrového alebo kolenného kĺbu) a:
- má závažné ochorenie srdca
- máte vážne problémy s žilami a tepnami
- ste nedávno mali srdcový infarkt alebo mozgovú príhodu
- nemôže užívať lieky na riedenie krvi
EPREX nemusí byť pre vás vhodný. Porozprávajte sa o tom so svojím lekárom. Počas používania lieku EPREX môžu niektorí ľudia potrebovať lieky na zníženie rizika vzniku krvných zrazenín. Ak nemôžete užívať antikoagulačné lieky, nemali by ste užívať liek EPREX.
Opatrenia pri používaní Čo potrebujete vedieť predtým, ako užijete Eprex
Buďte zvlášť opatrný pri EPREX
EPREX a ďalšie látky stimulujúce červené krvinky môžu u všetkých pacientov zvýšiť riziko vzniku krvných zrazenín.Toto riziko môže byť vyššie, ak máte iné rizikové faktory pre tvorbu krvných zrazenín (napríklad ak ste v minulosti mali krvnú zrazeninu alebo máte nadváhu, cukrovku, srdcové choroby alebo ste boli dlhodobo imobilizovaný kvôli chirurgický zákrok alebo choroba). Povedzte svojmu lekárovi o ktorejkoľvek z týchto vecí. Váš lekár vám pomôže rozhodnúť sa, či je EPREX pre vás to pravé.
Je dôležité, aby ste sa porozprávali so svojím lekárom, ak sa vás týka niečo z nasledujúceho.
EPREX môžete stále používať, ale najskôr by ste sa o tom mali porozprávať so svojím lekárom.
- Ak viete, že vás bolí alebo ste trpeli:
- Vysoký krvný tlak;
- Záchvaty alebo záchvaty
- Ochorenie pečene;
- Anémia z iných príčin;
- Porfýria (zriedkavá krvná porucha).
- Ak máte rakovinu, mali by ste si byť vedomí toho, že látky, ktoré stimulujú tvorbu červených krviniek (napríklad EPREX), môžu pôsobiť ako rastový faktor a teoreticky ovplyvniť progresiu nádoru. V závislosti od vášho individuálneho stavu môže byť vhodnejšia transfúzia krvi. Diskutujte o tom so svojim lekárom.
Osobitnú pozornosť venujte látkam, ktoré stimulujú tvorbu červených krviniek:
EPREX patrí do skupiny látok, ktoré ako ľudské erytropoetické faktory stimulujú tvorbu červených krviniek. Lekár sa vždy postará o zaznamenanie presného názvu produktu, ktorý používa. Ak vám počas liečby bude podávaná látka patriaca do tej istej skupiny, ale odlišná od lieku EPREX, pred použitím sa obráťte na svojho lekára alebo lekárnika.
Interakcie Ktoré lieky alebo potraviny môžu zmeniť účinok Eprexu
EPREX bežne neruší iné lieky, ale vždy informujte svojho lekára, ak užívate alebo ste v poslednom čase užívali ešte iné lieky, vrátane liekov, ktorých výdaj nie je viazaný na lekársky predpis.
Ak užívate liek nazývaný cyklosporín (používa sa napríklad po transplantácii obličky), lekár vám môže počas liečby EPREXom nariadiť krvné testy na kontrolu hladín cyklosporínu.
Doplnky železa a ďalšie antianemické faktory môžu zvýšiť účinnosť EPREXU. Váš lekár rozhodne, či ich máte užívať.
V prípade hospitalizácie alebo lekárskeho vyšetrenia, prosím, informujte, že ste liečený EPREXOM. To môže ovplyvniť iné ošetrenia alebo výsledky testov.
Upozornenia Je dôležité vedieť, že:
Tehotenstvo a dojčenie
Je dôležité povedať svojmu lekárovi, ak sa vás týka niektorý z nasledujúcich stavov. EPREX môžete stále používať, ale najskôr sa o tom porozprávajte so svojím lekárom.
- Ak ste tehotná alebo si myslíte, že by ste mohli byť.
- Ak dojčíte.
Dávka, spôsob a čas podávania Ako používať Eprex: Dávkovanie
Vždy používajte tento liek presne podľa pokynov lekára. Ak si nie ste niečím istý, overte si to u svojho lekára.
Váš lekár na základe vašich krvných testov určil, že potrebujete EPREX.
EPREX sa môže podávať injekčne:
- Do žily alebo trubice do žily (vnútrožilovo)
- Pod kožou (subkutánne)
Váš lekár rozhodne, ako sa má EPREX podávať. Injekcie obvykle podáva lekár, zdravotná sestra alebo zdravotnícky pracovník; niektorí ľudia sa môžu naučiť podávať liek subkutánne sami: pozri Pokyny na injekčné podanie lieku EPREX sami.
- Eprex sa nesmie používať:
- po dátume exspirácie uvedenom na štítku alebo vonkajšom obale
- ak viete alebo si myslíte, že liek mohol byť omylom zmrazený alebo áno
- a došlo k poruche chladničky
Dávka EPREXU je založená na vašej telesnej hmotnosti v kilogramoch a zvolí ju váš lekár v závislosti od príčiny anémie.
Váš lekár vám bude počas liečby EPREXom pravidelne kontrolovať krvný tlak.
Pacienti s renálnou insuficienciou
- Vaša hodnota hemoglobínu sa bude udržiavať medzi 10 a 12 g / dl, pretože vyššie hladiny hemoglobínu môžu zvýšiť riziko trombózy a smrti.
- Zvyčajná počiatočná dávka EPREXU pre dospelých alebo deti je 50 medzinárodných jednotiek (IU) na kilogram (/ kg) telesnej hmotnosti, podávaná 3 -krát týždenne.
- U pacientov na peritoneálnej dialýze sa podávanie môže vykonávať dvakrát týždenne.
- EPREX sa podáva intravenózne (žilou alebo hadičkou do žily) dospelým a deťom. Ak intravenózna cesta (žila alebo hadička do žily) nie je k dispozícii, váš lekár môže rozhodnúť, či si podám EPREX pod kožu (subkutánne). Vrátane dialyzovaných pacientov a pacientov, ktorí ešte nie sú na dialýze.
- Váš lekár vám bude pravidelne robiť krvné testy, aby zistil, či vaša anémia reaguje, a môže upraviť dávku, zvyčajne nie častejšie ako raz za 4 týždne.
- Akonáhle sa anémia upraví, váš lekár bude pravidelne kontrolovať vaše krvné testy. Dávku EPREXU a frekvenciu podávania je možné ďalej upravovať, aby sa udržala odpoveď na liečbu.
- Ak sa liečite liekom EPREX v dlhších intervaloch dávok (viac ako raz za týždeň), je možné, že nebudete schopní adekvátne udržať hladinu hemoglobínu a budete musieť zvýšiť dávku EPREXu alebo frekvenciu podávania.
- Aby bola liečba efektívnejšia, môžu vám byť pred a počas liečby EPREXOM užitočné doplnky železa.
- Ak ste na začiatku liečby EPREXOM na hemodialýze, bude možno potrebné upraviť váš dialyzačný režim. Lekár rozhodne.
Dospelí pacienti na chemoterapii
- Váš lekár môže začať liečbu EPREXOM, ak je hladina vášho hemoglobínu 10 g / dl alebo nižšia.
- Vaša hodnota hemoglobínu bude udržiavaná medzi 10 a 12 g / dl, pretože vyššie hladiny hemoglobínu môžu zvýšiť riziko trombózy a smrti.
- Počiatočná dávka je 150 IU na kilogram telesnej hmotnosti 3 -krát týždenne alebo 450 IU na kilogram telesnej hmotnosti raz za týždeň.
- EPREX sa podáva subkutánnou injekciou.
- Váš lekár vám bude pravidelne robiť krvné testy a môže upraviť dávku v závislosti od vašej odpovede na liečbu EPREXOM.
- Aby bola liečba efektívnejšia, môže byť pred a počas liečby EPREXOM pre vás užitočný doplnok železa.
- Liečba EPREXom obvykle pokračuje 1 mesiac po ukončení chemoterapie.
Dospelí pacienti, ktorí vkladajú vlastnú krv
- Zvyčajná dávka je 600 IU na kilogram telesnej hmotnosti 2 -krát týždenne.
- EPREX sa podáva do žily bezprostredne po uložení krvi 3 týždne pred operáciou.
- Aby bola liečba efektívnejšia, môže vám byť užitočný doplnok železa pred a počas liečby EPREXOM.
Dospelí pacienti, ktorí sú kandidátmi na veľkú ortopedickú chirurgiu
- Odporúčaná dávka je 600 IU na kilogram telesnej hmotnosti raz týždenne.
- EPREX sa podáva subkutánnou injekciou každý týždeň počas 3 týždňov pred operáciou a v deň operácie.
- Ak je potrebné skrátiť čas pred chirurgickým zákrokom, dostanete dennú dávku 300 IU / kg počas 10 dní pred chirurgickým zákrokom, v deň chirurgického zákroku a 4 dni po chirurgickom zákroku.
- Ak krvné testy pred operáciou odhalia príliš vysoké hodnoty hemoglobínu, liečba sa zastaví.
- Aby bola liečba efektívnejšia, môžu vám byť pred a počas liečby EPREXom užitočné doplnky železa.
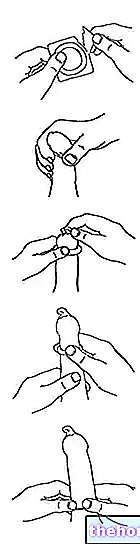
Pokyny na injekčné podanie lieku EPREX sami
- Na začiatku liečby liek EPREX zvyčajne podáva lekár alebo zdravotná sestra. Potom vám lekár môže navrhnúť, aby ste sa vy (alebo váš opatrovateľ) naučili, ako si podať injekciu (subkutánne).
- Nepokúšajte sa podať si injekciu, ak vám váš lekár alebo sestra nepovedali ako.
- Vždy sa riaďte pokynmi, ktoré vám dal váš lekár alebo zdravotná sestra.
- EPREX používajte iba vtedy, ak bol správne uložený - pozri časť Ako uchovávať EPREX
- Pred použitím vyberte injekčnú striekačku Eprex z chladničky a nechajte ju dosiahnuť izbovú teplotu. Obvykle to trvá 15-30 minút.
Odoberte jednu dávku EPREXU z každej naplnenej injekčnej striekačky. Keď sa EPREX podáva pod kožu (subkutánne), objem normálne neprekročí 1 mililiter (1 ml) pre každú jednotlivú injekciu.
EPREX sa musí podávať samotný a nesmie sa miešať s inými injekčnými tekutinami.
Naplnené injekčné striekačky EPREX netraste. Dlhodobé prudké trepanie môže výrobok poškodiť. Nepoužívajte výrobok, ak bol silne pretrepaný.
Ako si podať injekciu pomocou naplnených injekčných striekačiek
Naplnené injekčné striekačky sú vybavené bezpečnostným zariadením na ihly PROTECS ™, aby sa zabránilo riziku prilepenia ihly po použití. Toto je uvedené na obale.
- Pred použitím vyberte naplnenú injekčnú striekačku z chladničky. Tekutina musí dosiahnuť izbovú teplotu. Neodstraňujte kryt ihly, kým počkáte, kým dosiahne izbovú teplotu.
- Skontrolujte naplnenú injekčnú striekačku, aby ste sa presvedčili, či je správna dávka, či nevypršala doba použiteľnosti, či nie je poškodená a či je tekutina číra a nezmrazená.
- Vyberte miesto vpichu. Najvhodnejšími miestami na podanie injekcie sú stehno a brucho, okrem oblasti okolo pupka. Zakaždým zmeňte miesto vpichu.
- Na umývanie rúk. Na dezinfekciu miesta vpichu použite antiseptický obrúsok.
- Naplnenú injekčnú striekačku držte za valec injekčnej striekačky tak, aby zakrytá ihla smerovala nahor.
- Nedržte za hlavu piestu, piest, krídlo ochranného krytu ihly alebo kryt ochranného krytu ihly.
- Za žiadnych okolností neťahajte piest
- Neodstraňujte kryt ihly naplnenej injekčnej striekačky, kým nie ste pripravený podať EPREX
- Odstráňte ochranný kryt z ihly injekčnej striekačky tak, že ho držíte za telo a potiahnete za neho bez otáčania. Nestláčajte piest, nedotýkajte sa ihly ani netraste striekačkou. - Nedotýkajte sa aktivačných spôn bezpečnostného zariadenia, aby ste predišli predčasnému zakrytiu ihly ochrannou klapkou ihly
- Zdvihnite pokožku medzi palec a ukazovák bez toho, aby ste ju príliš stlačili.
- Zatlačte ihlu úplne dovnútra. Váš lekár alebo zdravotná sestra vám ukážu, ako na to.
- Zatláčajte piest palcom, kým sa nevstrekne celé množstvo tekutiny zodpovedajúce správnej dávke. Zatlačte pomaly a rovnomerne, pričom držte kožu vyvýšenú. Bezpečnostné zariadenie ihly PROTECS ™ sa neaktivuje, kým sa injekcia nepodá. Dávka úplne. Keď je aktivované bezpečnostné zariadenie ihly PROTECS ™, môžete počuť „cvaknutie“.
- Keď piest dosiahne koniec svojho zdvihu, vytiahnite ihlu a uvoľnite kožu.
- Pomaly vyberte palec z piesta, aby bola ihla úplne zakrytá bezpečnostným zariadením.
- Na konci injekcie môže byť v mieste vpichu malé množstvo krvi. To je normálne. Miesto vpichu môžete dezinfikovať stlačením antiseptického tampónu na niekoľko sekúnd.
- Použité injekčné striekačky zahoďte do bezpečného obalu - pozri časť Ako uchovávať Eprex
Predávkovanie Čo robiť, ak ste užili príliš veľa Eprexu
Ak použijete viac EPREXU, ako máte
Ak si myslíte, že ste použili príliš veľa EPREXU, povedzte to ihneď svojmu lekárovi alebo zdravotnej sestre.Žiaduce účinky pri predávkovaní sú nepravdepodobné.
Ak zabudnete podať EPREX
Vykonajte nasledujúcu injekciu hneď, ako si spomeniete. Ak ďalšia injekcia spadne do jedného dňa, preskočte vynechanú dávku a pokračujte podľa obvyklého plánu. Nezdvojnásobujte injekcie.
Ak ste pacient s hepatitídou C a dostávate interferón a ribavirín
Mali by ste navštíviť lekára, pretože kombinácia epoetínu alfa s interferónom a ribavirínom v zriedkavých prípadoch viedla k strate účinku a rozvoju závažnej formy anémie nazývanej čistá aplázia červených krviniek (PRCA). EPREX nie je schválený pre liečba anémie spojenej s hepatitídou C.
Ak máte ďalšie otázky týkajúce sa použitia tohto lieku, opýtajte sa svojho lekára, zdravotnej sestry alebo lekárnika.
Vedľajšie účinky Aké sú vedľajšie účinky lieku Eprex
Tak ako všetky lieky, aj EPREX môže spôsobovať vedľajšie účinky, hoci sa neprejavia u každého. Ak sa prejaví ktorýkoľvek z nižšie uvedených účinkov, ihneď to povedzte svojmu lekárovi alebo zdravotnej sestre.
Veľmi časté vedľajšie účinky
Vyskytujú sa u viac ako 1 z 10 pacientov používajúcich EPREX
- Hnačka
- Pocit nevoľnosti v žalúdku
- Zvracal
- Horúčka
- U pacientov s ochorením obličiek, ktorí ešte nepodstupujú dialýzu, bolo hlásené prekrvenie dýchacích ciest, ako je upchatý nos a bolesť hrdla.
Časté vedľajšie účinky
Tieto postihujú až 1 z 10 pacientov používajúcich EPREX
- Zvýšenie hodnôt krvného tlaku. Bolesť hlavy (najmä ak je náhla, akútna a podobná migréne) alebo zmätenosť alebo záchvaty. Môžu to byť príznaky náhleho zvýšenia krvného tlaku, ktoré si vyžaduje okamžitú liečbu. Zvýšenie krvného tlaku môže vyžadovať liečbu. Liekmi (alebo úprava dávky liekov, ktoré už užívate na vysoký krvný tlak).
- Krvné zrazeniny (vrátane hlbokej žilovej trombózy a embólie), ktoré môžu vyžadovať urgentnú liečbu. Príznakmi môžu byť bolesť na hrudníku, sipot, bolestivý opuch dolných končatín a začervenanie, zvyčajne v nohách.
- kašeľ.
- Podráždenie pokožky, ktoré môže byť spôsobené alergickou reakciou.
- Bolesť kostí alebo svalov.
- Chrípkový syndróm, ako je bolesť hlavy, bolesť kĺbov, pocit slabosti, zimnica, únava a závrat. Tieto reakcie sú bežnejšie na začiatku liečby. Ak sa u vás prejavia tieto príznaky pri podávaní injekcie do žily, pomalšie podávanie im môže pomôcť vyhnúť sa im v budúcnosti.
- Sčervenanie, pálenie a bolesť v mieste vpichu.
- Opuch členkov, chodidiel alebo prstov.
Menej časté vedľajšie účinky
Tieto postihujú až 1 z 100 pacientov používajúcich EPREX
- Vysoká hladina draslíka v krvi, ktorá môže spôsobiť abnormálny srdcový rytmus (to je veľmi častý vedľajší účinok u dialyzovaných pacientov).
- Kŕče
- Prekrvenie nosa alebo dýchacích ciest
Veľmi zriedkavé vedľajšie účinky
Tieto postihujú až 1 z 10 000 pacientov používajúcich EPREX
- Príznaky čistej aplázie červených krviniek (PRCA). PRCA znamená neschopnosť vytvárať dostatok červených krviniek v kostnej dreni. PRCA môže spôsobiť závažnú a náhlu anémiu, ktorej symptómy sú:
- neobvyklá únava,
- pocit závratu,
- dýchavičnosť
PRCA sa našla veľmi zriedkavo, obzvlášť u pacientov s ochorením obličiek po mesiacoch alebo rokoch liečby EPREXOM a inými látkami, ktoré stimulujú tvorbu červených krviniek. Zvlášť na začiatku liečby môže dôjsť k zvýšeniu hladiny malých krviniek (nazývaných krvné doštičky), ktoré sa bežne podieľajú na tvorbe zrazenín, nazývaných krvné doštičky. Váš lekár to skontroluje.
Ak ste na hemodialýze:
- V dialyzačnom skrate sa môžu vytvárať krvné zrazeniny (trombóza). To sa môže jednoduchšie stať, ak máte nízky krvný tlak (hypotenzia) alebo ak máte problémy s fistulou.
- V hemodialyzačnom systéme sa môžu vytvárať aj krvné zrazeniny. Váš lekár sa môže rozhodnúť zvýšiť dávku heparínu počas dialýzy.
Okamžite povedzte svojmu lekárovi alebo zdravotnej sestre, ak si všimnete niektorého z týchto účinkov alebo ak spozorujete akékoľvek iné účinky počas užívania EPREXU.
Ak začnete pociťovať akýkoľvek vedľajší účinok ako závažný alebo ak spozorujete vedľajšie účinky, ktoré nie sú uvedené v tejto písomnej informácii pre používateľov, povedzte to, prosím, svojmu lekárovi, zdravotnej sestre alebo lekárnikovi.
Pre tých, ktorí vykonávajú športové činnosti: používanie lieku bez terapeutickej potreby predstavuje doping a v každom prípade môže stanoviť pozitívne antidopingové testy.
Expirácia a retencia
Uchovávajte mimo dohľadu a dosahu detí.
Nepoužívajte tento liek po dátume exspirácie, ktorý je uvedený na škatuli a štítku po písmenách EXP. Dátum exspirácie je posledný deň v uvedenom mesiaci.
EPREX sa musí uchovávať v chladničke (2 ° C - 8 ° C).
EPREX je možné vybrať z chladničky a skladovať pri izbovej teplote (neprevyšujúcej 25 ° C) až 3 dni. Keď je naplnená injekčná striekačka vybratá z chladničky a dosiahne izbovú teplotu (neprevyšujúcu 25 ° C), musí sa použiť do 3 dní alebo sa musí zlikvidovať.
Nesmie byť zmrazené ani trepané
Uchovávajte v pôvodnom obale na ochranu pred svetlom.
Nepoužívajte tento liek, ak je uzáver poškodený alebo ak je roztok zafarbený alebo sú v ňom suspendované častice. Ak sú tieto podmienky pozorované, zlikvidujte liek
Lieky sa nesmú likvidovať odpadovou vodou alebo domovým odpadom. Opýtajte sa svojho lekárnika, ako zlikvidovať lieky, ktoré už nepoužívate. Pomôže to chrániť životné prostredie.
Obsah balenia a ďalšie informácie
Čo Eprex obsahuje
Účinnou látkou je: epoetín alfa (množstvo je uvedené v tabuľke nižšie).
Ďalšie zložky sú: polysorbát 80, chlorid sodný, dihydrát hydrogenfosforečnanu sodného, dihydrát hydrogenfosforečnanu sodného, glycín a voda na injekciu. Tento liek obsahuje menej ako 1 mmol sodíka (23 mg) v dávke, takže je v podstate bez sodíka.
Ako vyzerá EPREX a obsah balenia
EPREX je injekčný roztok v naplnených injekčných striekačkách. Predplnené injekčné striekačky sú vybavené bezpečnostným zariadením na ihly PROTECS ™ (pozri tabuľku nižšie) EPREX je číry a bezfarebný roztok.
Na trh nemusia byť uvedené všetky veľkosti balenia
Zdrojový leták: AIFA (Talianska agentúra pre lieky). Obsah zverejnený v januári 2016. Súčasné informácie nemusia byť aktuálne.
Aby ste mali prístup k najaktuálnejšej verzii, odporúča sa navštíviť webovú stránku AIFA (Talianska agentúra pre lieky). Vylúčenie zodpovednosti a užitočné informácie.
01.0 NÁZOV LIEKU
EPREX 10 000 IU / ML ROZTOK NA INJEKCIU Vo vopred naplnenej injekčnej striekačke
02.0 KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Epoetín alfa 10 000 IU / ml (84,0 µg / ml) vyrobený technológiou rekombinantnej DNA v bunkách vaječníkov čínskeho škrečka (CHO).
Jedna 0,3 ml naplnená injekčná striekačka obsahuje 3 000 IU (25,2 mcg) epoetínu alfa
Jedna 0,4 ml naplnená injekčná striekačka obsahuje 4 000 IU (33,6 mcg) epoetínu alfa
Jedna 0,5 ml naplnená injekčná striekačka obsahuje 5 000 IU (42,0 mcg) epoetínu alfa
Jedna 0,6 ml naplnená injekčná striekačka obsahuje 6 000 IU (50,4 mikrogramov) epoetínu alfa
Jedna 0,8 ml naplnená injekčná striekačka obsahuje 8 000 IU (67,2 mcg) epoetínu alfa
Jedna 1,0 ml naplnená injekčná striekačka obsahuje 10 000 IU (84,0 mcg) epoetínu alfa
Tento liek obsahuje menej ako 1 mmol (23 mg) sodíka v jednej dávke, tj. Je v zásade „bez sodíka“.
Úplný zoznam pomocných látok, pozri časť 6.1
03.0 LIEKOVÁ FORMA
Injekčný roztok v naplnených injekčných striekačkách
Číry, bezfarebný roztok
04.0 KLINICKÉ INFORMÁCIE
04.1 Terapeutické indikácie
EPREX je indikovaný na liečbu symptomatickej anémie spojenej s chronickým zlyhaním obličiek (CRI):
• u dospelých a pediatrických pacientov vo veku 1 - 18 rokov na hemodialýze a u dospelých pacientov na peritoneálnej dialýze.
• u dospelých pacientov s renálnou insuficienciou, ktorí ešte nepodstupujú dialýzu na liečbu závažnej anémie obličkového pôvodu sprevádzanej klinickými príznakmi u pacientov.
EPREX je indikovaný u dospelých pacientov, ktorí dostávajú chemoterapiu na solídne nádory, malígny lymfóm alebo mnohopočetný myelóm a u ktorých existuje riziko transfúzie, ako naznačuje celkový stav pacienta (kardiovaskulárna situácia, už existujúca anémia na začiatku chemoterapie) na liečbu anémie a redukcie o potrebe transfúzie.
EPREX je indikovaný u dospelých pacientov, ktorí sú súčasťou predonačného programu na zvýšenie množstva autológnej krvi. Liečba je indikovaná iba u pacientov so stredne ťažkou anémiou (koncentrácia hemoglobínu v rozmedzí Hb 10-13 g / dl [6, 2 - 8,1 mmol / l], bez nedostatku železa), ak nie sú k dispozícii postupy na uchovávanie krvi alebo sú nedostatočné v prípade veľkej elektívnej chirurgie vyžadujúcej veľké množstvo krvi (4 alebo viac jednotiek na ženy alebo 5 a viac jednotiek na mužov).
EPREX je indikovaný na zníženie expozície alogénnym krvným transfúziám u dospelých pacientov, ktorí nemajú nedostatok železa pred rozsiahlou plánovanou ortopedickou operáciou, o ktorej sa predpokladá, že má vysoké riziko komplikácií transfúzie. Použitie by malo byť obmedzené. U pacientov so stredne ťažkou anémiou (koncentrácia hemoglobínu) v rozmedzí Hb10-13 g / dl), pre ktorých nie je k dispozícii program autológneho darovania krvi a u ktorých sa očakáva mierna strata krvi (od 900 do 1 800 ml).
04.2 Dávkovanie a spôsob podávania
Dávkovanie
Pred začatím liečby epoetínom alfa a pri rozhodovaní o zvýšení dávky všetky ostatné príčiny anémie (nedostatok železa, folátu alebo vitamínu B12, intoxikácia hliníkom, infekcie alebo zápaly, strata krvi, hemolýza a fibróza kostnej drene akéhokoľvek pôvodu). Aby sa zaistila optimálna odpoveď na epoetín alfa, musia byť zaistené adekvátne zásoby železa a v prípade potreby podaná suplementácia železom (pozri časť 4.4).
Liečba symptomatickej anémie u dospelých pacientov s chronickým zlyhaním obličiek (CRI)
Príznaky a následky anémie sa môžu líšiť v závislosti od pohlavia, veku a prebiehajúcich sprievodných chorôb; je nevyhnutné, aby lekár zhodnotil klinický stav jednotlivého pacienta.
Požadovaná koncentrácia hemoglobínu je medzi 10 g / dl a 12 g / dl (6,2 až 7,5 mmol / l). EPREX sa má podávať tak, aby sa dosiahla koncentrácia hemoglobínu nepresahujúca 12 g / dl (7,5 mmol / l). Je potrebné vyhnúť sa zvýšeniu hemoglobínu o viac ako 2 g / dl (1,25 mmol / l) počas štvortýždňového obdobia. Ak k tomu dôjde, je potrebné primerane upraviť dávku.
Vzhľadom na variabilitu medzi pacientmi možno u pacienta príležitostne pozorovať hodnoty hemoglobínu nad a pod požadovanou koncentráciou hemoglobínu. Túto variabilitu je potrebné zvládnuť úpravou dávky, pričom sa rešpektuje rozsah koncentrácie hemoglobínu medzi 10 g / dl (6,2 mmol / l) a 12 g / dl (7,5 mmol / l).
Je potrebné sa vyhnúť hladine hemoglobínu trvalo nad 12 g / dl (7,5 mmol). Ak sa hemoglobín zvýši o viac ako 2 g / dl (1,25 mmol / l) za mesiac alebo ak hladina hemoglobínu trvalo presahuje 12 g / dl (7,5 mmol), znížte dávku EPREXU o 25%. Ak hemoglobín prekročí 13 g / dl ( 8,1 mmol / l), pozastavte terapiu, kým sa nevráti na 12 g / dl (7,5 mmol / l) a potom pokračujte v užívaní EPREXu v dávkach o 25% nižších ako predchádzajúce.
Pacienti majú byť starostlivo monitorovaní, aby sa zaistilo, že sa použije najnižšia schválená účinná dávka EPREXu, aby sa zabezpečila adekvátna kontrola anémie a súvisiacich symptómov udržaním koncentrácie hemoglobínu pod alebo rovnajúcou sa 12 g / dl (7, 5 mmol / l).
Pri zvyšovaní dávky ESA u pacientov s chronickým zlyhaním obličiek je potrebná opatrnosť. U pacientov so slabou odpoveďou hemoglobínu na ESA je potrebné hľadať alternatívnu príčinu slabej odpovede (pozri časti 4.4 a 5.1).
Ošetrenie EPREX je rozdelené na dve fázy - fázu korekčnú a fázu udržiavaciu.
Dospelí pacienti na hemodialýze
U hemodialyzovaných pacientov, kde je ľahko dostupný žilový prístup, je výhodnejšie použitie intravenózneho podania.
Korekčná fáza :
Počiatočná dávka je 50 IU / kg hmotnosti 3 -krát týždenne.
Ak je to potrebné, zvýšte alebo znížte dávku o 25 IU / kg (3 -krát týždenne), až kým sa nedosiahne požadovaná koncentrácia hemoglobínu v rozsahu 10 g / dl až 12 g / dl (6,2 až 7,5 mmol / l) (toto sa musí vykonať postupne v intervaloch najmenej štyroch týždňov).
- Fáza údržby :
Odporúčaná celková týždenná dávka je medzi 75 IU / kg a 300 IU / kg.
Má sa vykonať vhodná úprava dávky, aby sa hodnoty hemoglobínu udržali v rámci požadovanej koncentrácie hemoglobínu medzi 10 g / dl a 12 g / dl (6,2 až 7,5 mmol / l).
Pacienti s veľmi nízkou počiatočnou hladinou hemoglobínu (8 g / dl alebo> 5 mmol / l).
Dospelí pacienti s renálnou insuficienciou, ktorí ešte nepodstupujú dialýzu
U pacientov, kde žilový prístup nie je ľahko dostupný, je možné EPREX podať subkutánne.
Korekčná fáza
Počiatočná dávka je 50 IU / kg hmotnosti, 3 -krát týždenne, v prípade potreby nasleduje zvýšenie dávky o 25 IU / kg (3 -krát týždenne), kým sa nedosiahne požadovaná koncentrácia hemoglobínu (toto by sa malo vykonávať postupne v intervaloch najmenej štyroch týždňov).
Fáza údržby
Počas udržiavacej fázy sa EPREX môže podávať buď 3 -krát týždenne, a v prípade subkutánneho podávania jedenkrát týždenne alebo raz za dva týždne.
Dávka a dávkovacie intervaly sa musia správne nastaviť, aby sa hodnoty hemoglobínu udržali na požadovanej úrovni: Hb medzi 10 a 12 g / dl (6,2-7,5 mmol / l). Predĺženie dávkovacieho intervalu môže vyžadovať zvýšenie dávky.
Maximálna dávka by nemala presiahnuť 150 IU / kg 3 -krát týždenne, 240 IU / kg (až do maximálne 20 000 IU) jedenkrát týždenne alebo 480 IU / kg (do maximálne 40 000 IU) raz za 2 týždne.
Dospelí pacienti na peritoneálnej dialýze
U pacientov, kde žilový prístup nie je ľahko dostupný, je možné EPREX podať subkutánne.
Korekčná fáza
Počiatočná dávka je 50 IU / kg, dvakrát týždenne.
Fáza údržby
Odporúčaná udržiavacia dávka je medzi 25 IU / kg a 50 IU / kg, dvakrát týždenne, rozdelená na 2 rovnaké podania.
Má sa vykonať vhodná úprava dávky, aby sa hodnoty hemoglobínu udržali na požadovanej úrovni: hemoglobín medzi 10 g / dl a 12 g / dl (6,2-7,5 mmol / l).
Liečba dospelých pacientov s anémiou vyvolanou chemoterapiou
Príznaky a následky anémie sa môžu líšiť v závislosti od veku, pohlavia a všeobecnej situácie ochorenia; je nevyhnutné, aby lekár zhodnotil klinický stav jednotlivého pacienta.
EPREX sa má podávať anemickým pacientom, napr. koncentrácia hemoglobínu ≤10 g / dl (6,2 mmol / l).
Počiatočná dávka je 150 IU / kg, podávaná subkutánne, 3 krát týždenne.
Alternatívne sa EPREX môže podávať subkutánne v počiatočnej dávke 450 IU / kg jedenkrát týždenne.
Má sa vykonať vhodná úprava dávky, aby sa hodnoty hemoglobínu udržali na požadovanej úrovni: hemoglobín medzi 10 g / dl a 12 g / dl (6,2-7,5 mmol / l).
Vzhľadom na variabilitu medzi pacientmi možno u pacienta príležitostne pozorovať hodnoty hemoglobínu nad a pod požadovanou koncentráciou hemoglobínu. Túto variabilitu je potrebné zvládnuť úpravou dávky, pričom sa rešpektuje požadovaný rozsah koncentrácie hemoglobínu medzi 10 g / dl (6,2 mmol / l) a 12 g / dl (7,5 mmol / l).
Je potrebné vyhnúť sa koncentrácii hemoglobínu trvale nad 12 g / dl (7,5 mmol). Pokyny na správnu úpravu dávky v prípade, že hemoglobín dosiahne koncentrácie nad 12 g / dl (7,5 mmol), sú uvedené nižšie.
Ak sa po 4 týždňoch liečby zvýši koncentrácia hemoglobínu najmenej o 1 g / dl (0,62 mmol / l) alebo sa počet retikulocytov zvýši o ≥ 40 000 buniek / µl oproti východiskovému stavu, dávka by mala zostať na úrovni 150 IU / kg 3 -krát za týždeň alebo 450 IU / kg raz za týždeň.
Ak je zvýšenie koncentrácie hemoglobínu
Ak bolo zvýšenie koncentrácie hemoglobínu
Úprava dávky na udržanie koncentrácií hemoglobínu medzi 10 g / dl - 12 g / dl
Ak sa koncentrácia hemoglobínu zvýši o viac ako 2 g / dl (1,25 mmol / l) za mesiac alebo ak hemoglobín prekročí 12 g / dl (7,5 mmol / l), znížte dávku EPREXU asi o 25 -50%.
Ak koncentrácia hemoglobínu prekročí 13 g / dl (8,1 mmol / l), prerušte liečbu, kým koncentrácia neklesne pod 12 g / dl (7,5 mmol / l), a potom pokračujte v liečbe EPREXOM v dávke o 25% nižšej ako predchádzajúca dávka.
Odporúčané dávkovanie je popísané v nasledujúcom diagrame:
Pacienti majú byť starostlivo monitorovaní, aby sa zaistilo, že na zaistenie adekvátnej kontroly symptómov anémie sa použije najnižšia schválená dávka činidiel stimulujúcich erytropoézu (ESA).
Liečba EPREX by mala pokračovať ešte jeden mesiac po ukončení chemoterapie.
Liečba dospelých pacientov, ktorí sú kandidátmi na chirurgický zákrok, ktoré sú súčasťou programu autológneho darovania krvi
Mierne anemickí pacienti (hematokrit medzi 33-39%) vyžadujúci predbežnú depozíciu 4 alebo viacerých jednotiek krvi majú byť liečení 600 IU / kg EPREXU intravenózne, dvakrát týždenne, počas 3 týždňov pred chirurgickým zákrokom.
EPREX sa má podať po ukončení postupu darovania krvi.
Liečba dospelých pacientov, ktorí sú kandidátmi na veľkú elektívnu ortopedickú chirurgiu
Odporúčaná dávka je 600 IU / kg EPREXU podávaného subkutánne, raz týždenne počas troch týždňov pred chirurgickým zákrokom (-21 dní, -14 dní a -7 dní) a v deň chirurgického zákroku.
Ak je zo zdravotného hľadiska nevyhnutné skrátiť čakaciu dobu pred operáciou na menej ako tri týždne, dávka 300 IU / kg lieku EPREX sa má podávať subkutánne denne počas 10 po sebe nasledujúcich dní. Pred chirurgickým zákrokom, v deň chirurgického zákroku a v 4 dni bezprostredne po ňom.
Ak hemoglobín dosiahne v predoperačnom období 15 g / dl alebo viac, podávanie EPREXU sa má prerušiť a nemajú sa podávať žiadne ďalšie dávky.
Pediatrická populácia
Liečba symptomatickej anémie u pacientov s chronickým zlyhaním obličiek na hemodialýze
Príznaky a následky anémie sa môžu líšiť v závislosti od veku, pohlavia a prebiehajúcich sprievodných chorôb; je nevyhnutné, aby lekár zhodnotil klinický stav jednotlivého pacienta.
U pediatrických pacientov je požadovaná koncentrácia hemoglobínu medzi 9,5 g / dl a 11 g / dl (5,9 až 6,8 mmol / l). EPREX sa má podávať tak, aby sa dosiahla koncentrácia hemoglobínu nepresahujúca 11 g / dl (6,8 mmol / l). Je potrebné vyhnúť sa zvýšeniu hemoglobínu o viac ako 2 g / dl (1,25 mmol / l) počas štvortýždňového obdobia. Ak k tomu dôjde, je potrebné primerane upraviť dávku.
Pacienti majú byť starostlivo sledovaní, aby sa zaistilo, že sa použije najnižšia autorizovaná dávka EPREXu, aby sa zabezpečila adekvátna kontrola anémie a súvisiacich symptómov.
Liečba EPREX je rozdelená do dvoch fáz: korekčná fáza a udržiavacia fáza.
U pediatrických pacientov na hemodialýze, kde je už k dispozícii intravenózny prístup, je vhodnejšie vnútrožilové podanie.
Korekčná fáza:
Počiatočná dávka je 50 IU / kg hmotnosti intravenózne, 3 krát týždenne.
Ak je to potrebné, zvýšte alebo znížte dávku o 25 IU / kg (3 -krát týždenne), kým sa nedosiahne požadovaná koncentrácia hemoglobínu v rozsahu 9,5 g / dl až 11 g / dl (5,9 až 6,8 mmol / l) (to by sa malo stať. postupne v intervale najmenej štyroch týždňov).
Fáza údržby :
Má sa vykonať vhodná úprava dávky, aby sa hodnoty hemoglobínu udržali v rámci požadovanej koncentrácie hemoglobínu medzi 9,5 g / dl a 11 g / dl (5,9 až 6,8 mmol / l).
Deti s telesnou hmotnosťou nižšou ako 30 kg spravidla vyžadujú vyššie udržiavacie dávky ako deti s telesnou hmotnosťou viac ako 30 kg a dospelí.
Pediatrickí pacienti s veľmi nízkou počiatočnou hladinou hemoglobínu (6,8 g / dl alebo> 4,25 mmol / l).
Liečba pediatrických pacientov s anémiou vyvolanou chemoterapiou.
Bezpečnosť a účinnosť EPREXU u pediatrických pacientov liečených chemoterapiou nebola stanovená.
Liečba detských chirurgických pacientov, ktorí sa zúčastňujú programu autológneho darovania
Bezpečnosť a účinnosť EPREXU u pediatrických pacientov nebola stanovená.
Nie sú k dispozícii žiadne údaje.
Liečba pediatrických pacientov čakajúcich na rozsiahlu ortopedickú chirurgiu
Bezpečnosť a účinnosť EPREXU u pediatrických pacientov nebola stanovená.
Nie sú k dispozícii žiadne údaje.
Spôsob podávania
Buďte opatrní pred manipuláciou alebo podávaním lieku.
Pred použitím nechajte striekačku EPREX odpočinúť, kým nedosiahne izbovú teplotu. Obvykle to trvá 15 až 30 minút.
Liečba symptomatickej anémie u dospelých pacientov s chronickým zlyhaním obličiek
U pacientov s chronickým zlyhaním obličiek, kde je bežne dostupný intravenózny prístup (hemodialyzovaní pacienti), je vhodnejšie vnútrožilové podanie EPREXU.
Ak nie je intravenózny prístup ľahko dostupný (pacienti, ktorí ešte nepodstupujú dialýzu a pacienti na peritoneálnej dialýze), EPREX sa môže podávať subkutánne.
Liečba dospelých pacientov s anémiou vyvolanou chemoterapiou.
EPREX sa má podávať subkutánne.
Liečba dospelých chirurgických pacientov, ktorí sa zúčastňujú programu autológneho darovania
EPREX sa musí podávať vnútrožilovo.
Liečba dospelých pacientov plánovaných na veľkú elektívnu ortopedickú chirurgiu
EPREX sa má podávať subkutánne.
Liečba symptomatickej anémie u pediatrických pacientov s chronickým zlyhaním obličiek na hemodialýze
U pediatrických pacientov s chronickým zlyhaním obličiek, kde je už k dispozícii intravenózny prístup (hemodialyzovaní pacienti), je vhodnejšie vnútrožilové podanie EPREXU.
Intravenózne podanie
Podanie by malo trvať najmenej 1-5 minút v závislosti od celkovej dávky.
U hemodialyzovaných pacientov môže byť bolusová injekcia podaná počas dialýzy adekvátnym venóznym prístupom na dialyzačnej linke. Alternatívne môže byť injekcia podaná na konci dialýzy prostredníctvom prístupu k fistule, po ktorej nasleduje podanie 10 ml. fyziologického roztoku na opláchnutie prístupových ciest a zaistenie uspokojivého zavedenia produktu do krvného obehu.
U pacientov, u ktorých sa vyskytli reakcie podobné chrípke, je vhodnejšie pomalšie podávanie (pozri časť 4.8).
Nepodávajte EPREX intravenóznou infúziou alebo v roztoku s inými liekmi.
Subkutánne podanie
Maximálny objem 1 ml v každom mieste vpichu by spravidla nemal byť prekročený. Pri väčších objemoch je potrebné zvoliť viac ako jedno miesto vpichu.
Injekcie sa majú podať do končatín alebo prednej brušnej steny.
V prípade, že sa lekár domnieva, že pacient alebo opatrovateľ je schopný podávať EPREX subkutánne bezpečne a primerane, je potrebné poskytnúť pokyny pre správnu dávku a podanie.
Rovnako ako u iných injekčných liekov, skontrolujte, či v roztoku nie sú žiadne častice alebo farebné odchýlky.
04.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
Pacienti, u ktorých sa po liečbe akýmkoľvek erytropoetínom vyvinie čistá aplázia červených krviniek (PRCA), by nemali byť liečení liekom EPREX alebo inými erytropoetínmi (pozri časť 4.4 PRCA).
Nekontrolovaná hypertenzia.
U pacientov liečených EPREXOM je potrebné mať na pamäti všetky kontraindikácie súvisiace s programom autológneho pre-depozície krvi.
Použitie EPREXU je kontraindikované v prítomnosti závažných cievnych porúch na koronárnej, periférnej arteriálnej, karotickej alebo cerebrálnej úrovni u pacientov, ktorí sú kandidátmi na rozsiahlu ortopedickú chirurgiu a nie sú súčasťou programu autológneho darcovstva. Použitie je tiež kontraindikované. u pacientov s nedávnymi epizódami infarktu myokardu alebo inými cerebrovaskulárnymi komplikáciami.
Pacienti, ktorí sú kandidátmi na chirurgický zákrok a ktorí z akéhokoľvek dôvodu nemôžu dostať adekvátnu antitrombotickú profylaxiu.
04.4 Špeciálne upozornenia a vhodné opatrenia pri používaní
Generál
U všetkých pacientov, ktorí dostávajú epoetín alfa, má byť krvný tlak starostlivo monitorovaný a podľa potreby kontrolovaný. Epoetín alfa sa má používať opatrne v prítomnosti neliečenej, nedostatočne liečenej alebo ťažko kontrolovateľnej hypertenzie. Možno bude potrebné začať alebo zintenzívniť antihypertenzívnu liečbu. Ak nie je možné kontrolovať krvný tlak, liečba epoetínom alfa sa má ukončiť.
Počas liečby epoetínom alfa sa vyskytli hypertenzívne krízy s encefalopatiou a záchvatmi, vyžadujúce okamžitú lekársku pomoc a intenzívnu lekársku starostlivosť, dokonca aj u pacientov s predchádzajúcim normálnym alebo nízkym krvným tlakom. Osobitnú pozornosť treba venovať záchvatom podobným migréne ako možnému varovnému znaku (pozri časť 4.8).
Epoetin alfa sa má používať opatrne u pacientov s epilepsiou, záchvatmi v anamnéze alebo so zdravotnými stavmi spojenými s predispozíciou k záchvatovej aktivite, ako sú infekcie centrálneho nervového systému a mozgové metastázy.
Epoetín alfa sa má používať s opatrnosťou u pacientov s chronickou hepatálnou insuficienciou.Bezpečnosť epoetínu alfa nebola stanovená u pacientov s hepatálnou dysfunkciou.
U pacientov, ktorí dostávali ESA, bol pozorovaný zvýšený výskyt vaskulárnych trombotických príhod (VTE) (pozri časť 4.8). Patria sem venózna a arteriálna trombóza a embólia (vrátane niektorých s fatálnymi následkami), ako je hlboká žilová trombóza, pľúcna embólia, sietnica trombóza a infarkt myokardu Okrem toho boli hlásené cerebrovaskulárne príhody (vrátane mozgového infarktu, mozgového krvácania a prechodných ischemických záchvatov).
Riziko týchto VTE je potrebné starostlivo zvážiť v porovnaní s prínosom liečby epoetínom alfa, najmä u pacientov s už existujúcimi rizikovými faktormi VTE vrátane obezity a predchádzajúcej VTE (napr. Trombóza hlbokých žíl, pľúcna embólia a cerebrovaskulárne príhody)
Hladiny hemoglobínu sa majú u všetkých pacientov starostlivo monitorovať kvôli potenciálnemu zvýšenému riziku tromboembolických príhod a smrteľných následkov, keď sú pacienti liečení hladinami hemoglobínu nad uvedenú koncentráciu.
Počas liečby epoetínom alfa sa môže vyskytnúť mierne na dávke závislé zvýšenie počtu krvných doštičiek, aj keď v normálnom rozmedzí. Tento jav počas terapie ustupuje. Okrem toho bola hlásená trombocytémia nad normálnym rozsahom. Odporúča sa pravidelné monitorovanie krvných doštičiek počas prvých 8 týždňov terapie.
Pred začatím liečby epoetínom alfa a pri rozhodovaní je potrebné vyhodnotiť a liečiť všetky možné príčiny anémie (nedostatok železa, nedostatok folátu alebo vitamínu B12, otravu hliníkom, infekciu alebo zápal, stratu krvi, hemolýzu a fibrózu kostnej drene akéhokoľvek pôvodu). je vyrobený na zvýšenie dávky. Vo väčšine prípadov sa hodnoty feritínu v sére znižujú súčasne so zvyšovaním hodnôt hematokritu. Aby sa zabezpečila optimálna odpoveď na epoetín alfa, mali by sa zabezpečiť dostatočné zásoby železa a v prípade potreby sa majú podať doplnky železa ( pozri časť 4.2):
• U pacientov s chronickým zlyhaním obličiek sa odporúča doplnenie železa, ak sú hladiny feritínu nižšie ako 100 ng / ml (elementárne železo pre dospelých 200 až 300 mg / deň perorálne a pre deti od 100 do 200 mg / deň perorálne).
• U pacientov s rakovinou sa odporúča doplnenie železa, ak sú hodnoty saturácie transferínu nižšie ako 20% (elementárne železo 200 až 300 mg / deň orálne).
• U pacientov v programe autológneho darovania darčekov by sa mala podávať suplementácia železom (elementárne železo 200 mg / deň perorálne) niekoľko týždňov pred začiatkom autológnej darovania, aby sa dosiahli vysoké zásoby železa. Pred začatím liečby epoetínom alfa a počas kurzu terapia epoetínom alfa.
• U pacientov plánovaných na rozsiahlu ortopedickú chirurgiu by sa počas liečby epoetínom alfa mala podávať suplementácia železom (elementárne železo 200 mg / deň perorálne). „Suplementácia železom pred začatím terapie epoetínom alfa, aby sa dosiahla adekvátna rezerva železa.
U pacientov liečených epoetínom alfa bol veľmi zriedkavo pozorovaný nástup alebo zhoršenie porfýrie.
Epoetín alfa sa má používať s opatrnosťou u pacientov s porfýriou.
Aby sa zabezpečila vysledovateľnosť stimulačných činidiel erytropoézy (ESA), musí byť obchodný názov podávaného ESA vždy zaregistrovaný alebo uvedený v zdravotnej dokumentácii pacienta.
Zmena terapie z jedného ESA na druhý by sa mala vykonávať iba pod príslušným dohľadom.
Čistá aplázia červených krviniek (PRCA)
Protilátkami sprostredkovaná čistá aplázia červených krviniek (PRCA) bola hlásená po mesiacoch až rokoch, hlavne u pacientov s chronickým zlyhaním obličiek liečených epoetínom podávaným subkutánne.
Prípady boli hlásené aj u pacientov s hepatitídou C liečených interferónom a ribavirínom, ak boli podávané v kombinácii s ESA. Epoetin alfa nie je schválený na liečbu anémie spojenej s hepatitídou C.
U pacientov, ktorí vykazujú náhlu stratu účinnosti, definovanú ako pokles hodnôt hemoglobínu (1 až 2 g / dl za mesiac) so zvýšenou potrebou transfúzií, by sa mal vykonať počet retikulocytov a vyhodnotiť známe príčiny. Ktoré bránia reakcia (ako je nedostatok železa, folátu a vitamínu B12, intoxikácia hliníkom, infekcia alebo zápal, strata krvi, hemolýza a fibróza kostnej drene akéhokoľvek pôvodu).
Neúmerné zníženie hodnôt hemoglobínu a rozvoj závažnej anémie súvisiacej s nízkym počtom retikulocytov by mali viesť k prerušeniu liečby epoetínom alfa a vykonať test na prítomnosť antierytropoetínových protilátok.
Tiež by sa malo zvážiť vyšetrenie kostnej drene na diagnostiku PRCA.
Nemala by sa začať žiadna liečba inými ESA kvôli riziku skríženej reakcie.
Liečba symptomatickej anémie u dospelých a pediatrických pacientov s chronickým zlyhaním obličiek (CRI):
Pacientom s chronickým zlyhaním obličiek, ktorí dostávajú epoetín alfa, by sa mali pravidelne merať hladiny hemoglobínu, kým sa nedosiahne stabilná hladina, a potom sa majú pravidelne merať.
U pacientov s chronickým zlyhaním obličiek na zníženie rizika zvýšenia krvného tlaku by sa mal hemoglobín zvýšiť približne o 1 g / dl / mesiac (0,62 mmol / l) a nemal by prekročiť 2 g / dl / mesiac (1,25 mmol / l).
U pacientov s chronickou renálnou insuficienciou by udržiavacia koncentrácia hemoglobínu nemala prekročiť maximálnu hodnotu rozsahu koncentrácií hemoglobínu, ako je uvedené v časti 4.2. V klinických skúšaniach, keď boli podávané látky stimulujúce erytropoézu (ESA), bolo pozorované zvýšené riziko úmrtnosti a závažných kardiovaskulárnych príhod. podávaný tak, aby sa dosiahla hladina koncentrácie hemoglobínu nad 12 g / dl (7,5 mmol / ml).
Kontrolované klinické štúdie nepreukázali žiadny významný prínos pri podávaní epoetínov, keď koncentrácia hemoglobínu prekročí úroveň potrebnú na kontrolu symptómov anémie a zabránenie transfúzii krvi.
Pri zvyšovaní dávky EPREXU u pacientov s chronickým zlyhaním obličiek je potrebná opatrnosť, pretože vysoké kumulatívne dávky epoetínu môžu byť spojené so zvýšeným rizikom úmrtnosti, závažných kardiovaskulárnych a cerebrovaskulárnych príhod. U pacientov so slabou odpoveďou hemoglobínu na epoetíny je alternatívou treba hľadať príčinu tejto zlej reakcie (pozri časti 4.2 a 5.1).
U pacientov s chronickým zlyhaním obličiek liečených subkutánnym epoetínom alfa je potrebné pravidelne monitorovať stratu účinnosti, to znamená absenciu alebo zníženú odpoveď na epoetín alfa u pacientov, ktorí predtým odpovedali na liečbu. Tento jav je charakterizovaný trvalým poklesom hodnôt hemoglobínu v porovnaní so zvýšením dávky epoetínu alfa (pozri časť 4.8).
Niektorí pacienti liečení epoetínom alfa v dlhších dávkovacích intervaloch (viac ako raz týždenne) nemusia udržiavať dostatočné hladiny hemoglobínu (pozri časť 5.1) a môžu vyžadovať zvýšenie dávky. Hladiny hemoglobínu je potrebné pravidelne monitorovať.
Trombóza vaskulárnych prístupov sa vyskytla u hemodialyzovaných pacientov, najmä u pacientov so sklonom k hypotenzii a s komplikáciami arteriovenóznych fistúl (napr. Stenóza, aneuryzma atď.). U týchto pacientov sa odporúča preventívna kontrola vaskulárneho prístupu a profylaxia trombózy s podávaním napr. kyseliny acetylsalicylovej.
V ojedinelých prípadoch bola pozorovaná hyperkaliémia, aj keď kauzalita nebola stanovená. U pacientov s chronickým zlyhaním obličiek je potrebné monitorovať sérové elektrolyty. Ak sa pozorujú zvýšené (alebo stúpajúce) hladiny draslíka v sére, okrem vhodnej liečby hyperkaliémie sa má zvážiť prerušenie podávania epoetínu alfa, kým sa hladiny draslíka v sére neupravia.
Počas hemodialýzy je často potrebné zvýšenie dávky heparínu kvôli zvýšeniu hodnoty hematokritu. Ak úprava dávok heparínu nie je optimálna, môže dôjsť k oklúzii dialyzátora. Na základe doteraz dostupných údajov korekcia anémie epoetínom alfa u dospelých pacientov s chronickým zlyhaním obličiek, ktorí ešte nepodstupujú dialýzu, neurýchľuje progresiu zlyhania obličiek.
Liečba pacientov s anémiou vyvolanou chemoterapiou
Pacientom s rakovinou, ktorí dostávajú epoetín alfa, by sa mali pravidelne merať hladiny hemoglobínu, kým sa nedosiahne stabilná hladina, a potom sa majú pravidelne merať.
Erytropoetíny sú rastové faktory, ktoré v podstate stimulujú tvorbu červených krviniek. Erytropoetínové receptory môžu byť exprimované na povrchu rôznych rakovinových buniek. Rovnako ako u všetkých rastových faktorov existujú teoretické obavy, že erytropoetíny môžu stimulovať rast nádoru.
V niektorých kontrolovaných klinických skúšaniach nebolo dokázané, že erytropoetíny zlepšujú celkové prežitie alebo znižujú riziko progresie nádoru u pacientov s anémiou spojenou s nádorom.
V kontrolovaných klinických skúšaniach používanie epoetínu alfa a iných činidiel stimulujúcich erytropoézu (ESA) ukázalo:
• znížená lokoregionálna kontrola u pacientov s pokročilým karcinómom hlavy a krku, ktorí dostávajú rádioterapiu, keď sa podávajú, aby sa dosiahli hladiny hemoglobínu nad 14 g / dl (8,7 mmol / l);
• znížené celkové prežitie a zvýšená úmrtnosť súvisiaca s progresiou ochorenia po 4 mesiacoch u pacientok s metastatickým karcinómom prsníka, ktoré sú liečené chemoterapiou, aby sa dosiahli hladiny hemoglobínu medzi 12-14 g / dl (7,5-8,7 mmol / l);
• zvýšené riziko úmrtnosti pri podávaní na dosiahnutie hladín hemoglobínu 12 g / dl (7,5 mmol / l); u pacientov s aktívnou neopláziou, ktorí nepodstupujú chemoterapiu a / alebo rádioterapiu. Liečba činidlami stimulujúcimi erytropoézu (ESA) nie je v tejto populácii pacientov indikovaná.
Vzhľadom na uvedené skutočnosti má byť v niektorých klinických situáciách pri liečbe anémie u onkologických pacientov uprednostňovaná krvná transfúzia. Rozhodnutie o aplikácii rekombinantného erytropoetínu by malo byť založené na posúdení prínosu a rizika s individuálnym zapojením pacienta. Faktory, ktoré je potrebné vziať do úvahy pri tomto hodnotení, musia zahŕňať typ rakoviny a jej priebeh; stupeň anémie; dĺžka života; prostredie, v ktorom je pacient liečený; preferencie pacienta (pozri časť 5.1).
U pacientov s rakovinou, ktorí sú liečení chemoterapiou, je potrebné pri posudzovaní vhodnosti terapie epoetínom alfa (pacienti s rizikom transfúzie) starostlivo zvážiť 2-3 týždňový interval medzi podaním a výskytom červených krviniek indukovaných ESA.
Dospelí pacienti, ktorí sú kandidátmi na chirurgické zákroky, ktoré sú súčasťou programov darcovstva autológnej krvi
Musia byť dodržané všetky varovania a špeciálne opatrenia súvisiace s programom darovania autológnej krvi, obzvlášť rutinná výmena objemu.
Pacienti kandidáti na veľkú elektívnu ortopedickú chirurgiu
Predoperačne by ste mali vždy dodržiavať správne postupy správy krvi.
Pacienti, ktorí sú kandidátmi na elektívny veľký ortopedický chirurgický zákrok, by mali dostať „adekvátnu antitrombotickú profylaxiu, pretože u pacientov podstupujúcich chirurgický zákrok sa môžu vyskytnúť trombotické a cievne príhody, najmä u pacientov so základnými kardiovaskulárnymi poruchami. Okrem toho je potrebné u pacientov s predispozíciou prijať špeciálne opatrenia. vývoj hlbokej žilovej trombózy (DVT). Okrem toho u pacientov s „východiskovým hemoglobínom> 13 g / dl je možnosť, že liečba epoetínom alfa môže byť spojená so zvýšeným rizikom posttrombotických / cievnych príhod. operátorov nemožno vylúčiť . Epoetín alfa by preto nemal byť používaný u pacientov s východiskovými hodnotami hemoglobínu> 13 g / dl.
04.5 Interakcie s inými liekmi a iné formy interakcie
Neexistuje žiadny dôkaz, že liečba epoetínom alfa mení metabolizmus iných liekov. Lieky, ktoré znižujú erytropoézu, môžu znižovať odpoveď na epoetín alfa.
Pretože sa cyklosporín viaže na červené krvinky, môže dôjsť k „interakcii s týmto liekom.
V prípade súbežného podávania sa majú sledovať hladiny cyklosporínu v krvi a dávka sa má upraviť podľa zvýšenia hematokritu.
Neexistujú žiadne in vitro interakcie medzi G-CSF, GM-CSF a epoetínom alfa, pokiaľ ide o hematologickú diferenciáciu alebo proliferáciu in vitro vzoriek biopsie nádoru.
U dospelých pacientok s metastatickým karcinómom prsníka nemalo subkutánne súbežné podanie 40 000 IU / ml epoetínu alfa s trastuzumabom 6 mg / kg žiadny vplyv na farmakokinetiku trastuzumabu.
04.6 Gravidita a laktácia
Tehotenstvo
Neexistujú adekvátne a dobre kontrolované štúdie u tehotných žien. Štúdie na zvieratách preukázali reprodukčnú toxicitu (pozri časť 5.3). Epoetín alfa sa má preto používať v gravidite iba vtedy, ak očakávaný prínos preváži potenciálne riziko pre plod. Použitie epoetínu alfa sa neodporúča u gravidných žien, ktoré sú kandidátmi na chirurgický zákrok, ktoré sa zúčastňujú programu autológneho darcovstva krvi.
Čas kŕmenia
Nie je známe, či sa exogénny epoetín alfa vylučuje do ľudského materského mlieka. Epoetín alfa sa má používať s opatrnosťou u dojčiacich žien.Rozhodnutie pokračovať / prerušiť dojčenie alebo pokračovať / prerušiť liečbu epoetínom alfa sa musí urobiť po zvážení prínosu dojčenia pre dieťa a prínosu liečby epoetínom alfa pre ženu.
Použitie epoetínu alfa sa neodporúča u dojčiacich žien, ktoré sú kandidátmi na chirurgický zákrok, ktoré sa zúčastňujú programu autológneho darcovstva krvi.
Plodnosť
Neexistujú žiadne štúdie hodnotiace potenciálny účinok epoetínu alfa na mužskú alebo ženskú plodnosť.
04.7 Účinky na schopnosť viesť vozidlá a obsluhovať stroje
Neuskutočnili sa žiadne štúdie o schopnosti viesť vozidlá alebo obsluhovať stroje.
04.8 Nežiaduce účinky
Zhrnutie bezpečnostného profilu
Najčastejšou nežiaducou reakciou na liek počas liečby epoetínom alfa je zvýšenie krvného tlaku závislé od dávky alebo zhoršenie už existujúcej hypertenzie.
Zvlášť na začiatku liečby sa odporúča sledovať trend krvného tlaku (pozri časť 4.4).
Najčastejšími nežiaducimi reakciami na lieky, ktoré sa vyskytli v klinických štúdiách s epoetínom alfa, sú hnačka, nauzea, vracanie, pyrexia a bolesť hlavy. Príznaky podobné chrípke sa môžu objaviť prevažne na začiatku liečby.
V klinických štúdiách s predĺžením dávkovacieho rozsahu u dospelých pacientov s renálnou insuficienciou, ktorí ešte nepodstupujú dialýzu, bolo hlásené preťaženie dýchacieho traktu, vrátane preťaženia horných dýchacích ciest, upchatia nosa a rinofaryngitídy.
U pacientov, ktorí dostávali ESA, bol pozorovaný zvýšený výskyt vaskulárnych trombotických príhod (TVE) (pozri časť 4.4).
Tabuľka nežiaducich reakcií
Z celkového počtu 3 262 pacientov v 23 randomizovaných, dvojito zaslepených, placebom alebo štandardne kontrolovaných klinických štúdiách bol celkový bezpečnostný profil lieku EPREX hodnotený u 1 992 anemických pacientov. Do 4 štúdií chronického zlyhania obličiek bolo zaradených 228 pacientov s ICR liečených epoetínom alfa (2 štúdie pred dialýzou [N = 131 pacientov vystavených ICR] a 2 na dialýze [N = 97 pacientov vystavených ICR]); 1 404 pacientov s rakovinou vystavených v 16 štúdiách s anémiou spôsobenou chemoterapiou; 147 pacientov vystavených v 2 štúdiách na darovanie autológnej krvi a 213 pacientov vystavených v 1 štúdii v perioperačnom období. Nežiaduce reakcie hlásené u ≥ 1% pacientov liečených epoetín alfa v týchto klinických skúšaniach sú uvedené v tabuľke nižšie.
Nasledujúce definície platia pre rôzne frekvencie: veľmi časté (≥ 1/10), časté (≥ 1/100 až
Popis vybraných nežiaducich reakcií
Boli hlásené reakcie z precitlivenosti vrátane prípadov vyrážky (vrátane žihľavky), anafylaktických reakcií a angioedému.
Hypertenzívne krízy s encefalopatiou a záchvatmi, ktoré si vyžadovali okamžitú lekársku pomoc a intenzívnu lekársku starostlivosť, sa vyskytli počas liečby epoetínom alfa aj u pacientov s predchádzajúcim normálnym alebo nízkym krvným tlakom. Osobitnú pozornosť treba venovať záchvatom podobným migréne ako možnému varovnému znaku (pozri časť 4.4).
Protilátkami sprostredkovaná čistá aplázia červených krviniek bola veľmi zriedkavo hlásená u
Pediatrická populácia s chronickým zlyhaním obličiek na hemodialýze
Expozícia pediatrických pacientov s chronickým zlyhaním obličiek hemodialýzou v klinických štúdiách a po uvedení lieku na trh je obmedzená. V tejto populácii neboli hlásené žiadne špecifické nežiaduce účinky z pediatrickej populácie, ktoré nie sú uvedené v tabuľke vyššie, ani žiadne nežiaduce reakcie typické pre základné ochorenie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité, pretože umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia. "Adresa http: //www.agenziafarmaco.gov.it/it/responsabili.
04,9 Predávkovanie
Terapeutické rozpätie epoetínu alfa je veľmi široké. Predávkovanie epoetínom alfa môže vyvolať účinky, ktoré sú rozšírením farmakologických účinkov hormónu. Ak sa zistia nadmerne vysoké hladiny hemoglobínu, môže sa vykonať flebotómia.
Podľa stavu pacienta by mala byť poskytnutá dodatočná podporná starostlivosť.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antianemikum, ATC kód: B03XA01.
Mechanizmus akcie
Erytropoetín (EPO) je glykoproteínový hormón produkovaný predovšetkým obličkami v reakcii na hypoxiu a je kľúčovým regulátorom produkcie červených krviniek (RBC). "EPO sa podieľa na všetkých fázach vývoja erytroidov a má hlavný účinok na úrovni prekurzorov erytroidov. Potom, čo sa EPO naviaže na svoj receptor na povrchu bunky, aktivuje cesty prenosu signálu, ktoré interferujú s" apoptózou a stimulujú proliferáciu erytroidných buniek. Rekombinantný ľudský erytropoetín (epoetín alfa), exprimovaný v bunkách vaječníkov čínskeho škrečka, má sekvenciu 165 aminokyselín identických so sekvenciami ľudského EPO v moči; tieto 2 sú nerozlíšiteľné na základe funkčných testov. Zjavná molekulová hmotnosť erytropoetínu je medzi 32 000 a 40 000 daltony.
Erytropoetín je rastový faktor, ktorý primárne stimuluje produkciu erytrocytov. Erytropoetínové receptory môžu byť exprimované na povrchu rôznych rakovinových buniek.
Farmakodynamické účinky
Zdraví dobrovoľníci
Po jednorazových dávkach epoetínu alfa (20 000 až 160 000 IU subkutánne) sa u skúmaných farmakodynamických markerov vrátane: retikulocytov, červených krviniek a hemoglobínu pozorovala od dávky závislá odpoveď. Časovo definovaný koncentračný časový profil bol pozorovaný s vrcholom a návratom na východiskové hodnoty pre zmeny v percentách retikulocytov. Menej definovaný profil bol pozorovaný pre erytrocyty a hemoglobín. Vo všeobecnosti sa všetky farmakodynamické markery zvyšovali lineárne s dávkami dosahujúcimi maximálnu odpoveď pri maximálnych hladinách dávok.
Ďalšie farmakodynamické štúdie skúmali 40 000 IU raz za týždeň v porovnaní so 150 IU / kg 3 -krát za týždeň. Napriek rozdielom v časovom profile koncentrácie je farmakodynamická odpoveď (meraná percentuálnymi zmenami v retikulocytoch, hemoglobíne a celkových červených krvinkách) v týchto režimoch podobná. Ďalšie štúdie porovnávali režim 40 000 IU epoetínu alfa jedenkrát týždenne s dvojtýždennými dávkami v rozmedzí od 80 000 do 120 000 IU subkutánne. Celkovo sa na základe výsledkov týchto farmakodynamických štúdií na zdravých subjektoch zdá, že dávkovací režim 40 000 IU jedenkrát týždenne je účinnejší v produkcii červených krviniek ako dvojtýždenné napriek podobnosti v produkcii retikulocytov. Jedenkrát za týždeň a dvojtýždňové režimy.
Chronické zlyhanie obličiek
Ukázalo sa, že epoetín alfa stimuluje erytropoézu u anemických pacientov s chronickým zlyhaním obličiek, vrátane dialyzovaných a predialyzovaných pacientov.Prvým dôkazom reakcie na epoetín alfa je zvýšenie počtu retikulocytov do 10 dní, po ktorom nasleduje zvýšenie počtu červených krviniek, hemoglobínu a hematokritu, zvyčajne do 2 až 6 týždňov. Odozva hemoglobínu sa u pacientov líši a môže byť ovplyvnená usadeninami železa a prítomnosťou sprievodných zdravotných problémov.
Anémia vyvolaná chemoterapiou
Epoetín alfa podávaný 3 -krát týždenne alebo 1 -krát týždenne preukázateľne zvyšuje hemoglobín a znižuje potrebu transfúzií po prvom mesiaci liečby anemických pacientov s rakovinou, ktorí dostávajú chemoterapiu.
V štúdii porovnávajúcej režimy dávkovania 150 IU / kg 3 -krát týždenne a 40 000 IU jedenkrát týždenne u zdravých osôb a subjektov s anémiou s rakovinou boli časové profily percentuálnych zmien retikulocytov, hemoglobínu a celkových červených krviniek podobné medzi dva dávkovacie režimy u zdravých a anemických subjektov s rakovinou. AUC príslušných farmakodynamických parametrov boli podobné medzi dávkovacími režimami 150 IU / kg 3 -krát týždenne a 40 000 IU jedenkrát týždenne u zdravých aj anemických jedincov s rakovinou.
Dospelí chirurgickí pacienti v programe autológneho darovania
Ukázalo sa, že epoetín alfa stimuluje produkciu červených krviniek, aby sa zvýšil autológny odber krvi a obmedzil pokles hemoglobínu u dospelých pacientov plánovaných na veľký plánovaný chirurgický zákrok, u ktorých sa neočakáva úplné perioperačné predbežné skladovanie. Najväčšie účinky boli pozorované u pacientov s nízkymi hladinami hemoglobínu (≤ 13 g / dl).
Liečba dospelých pacientov plánovaných na veľkú elektívnu ortopedickú chirurgiu
U pacientov plánovaných na rozsiahlu ortopedickú operáciu s predbežným ošetrením hemoglobínu> 10 až ≤ 13 g / dl preukázalo, že epoetín alfa znižuje riziko podávania alogénnych transfúzií a urýchľuje obnovu erytroidu (zvýšené hladiny hemoglobínu, hematokritu a počtu retikulocytov).
Klinická účinnosť a bezpečnosť
Chronické zlyhanie obličiek
Epoetín alfa bol hodnotený v klinických skúškach u anemických dospelých pacientov s CRF, vrátane hemodialyzovaných a predialyzovaných pacientov, na liečbu anémie a udržanie hematokritu v rozmedzí koncentrácií 30 až 36%.
V klinických skúšaniach pri počiatočných dávkach 50 -150 IU / kg trikrát týždenne odpovedalo približne 95% všetkých pacientov s klinicky významným zvýšením hematokritu. Po približne dvoch mesiacoch liečby boli takmer všetci pacienti transfúziou. -Nezávislé. Raz keď bol dosiahnutý cieľ hematokritu, udržiavacia dávka bola prispôsobená pre každého pacienta.
V troch veľkých klinických skúšaniach u dospelých dialyzovaných pacientov bola priemerná udržiavacia dávka potrebná na udržanie hematokritu medzi 30 a 36% približne 75 IU / kg 3 -krát týždenne.
V dvojito zaslepenej, multicentrickej, placebom kontrolovanej štúdii kvality života pacientov s CRF na hemodialýze bolo preukázané klinicky a štatisticky významné zlepšenie u pacientov liečených epoetínom alfa v porovnaní so skupinou s placebom, meranie únavy, telesných symptómov, vzťahov a depresie (Dotazník ochorenia obličiek) po šiestich mesiacoch terapie. Pacienti v skupine s epoetínom alfa boli zaradení do otvorenej rozšírenej štúdie, ktorá preukázala, že zlepšenie kvality ich života bolo zachované ďalších 12 mesiacov.
Dospelí pacienti s renálnou insuficienciou, ktorí ešte nie sú na dialýze
V klinických štúdiách s pacientmi s CRF, ktorí neboli na dialýze a boli liečení epoetínom alfa, bola priemerná dĺžka liečby takmer päť mesiacov. Títo pacienti reagovali na liečbu epoetínom alfa podobným spôsobom, aký sa pozoroval u dialyzovaných pacientov. Pacienti s CRF, ktorí nie sú na dialýze, vykazovali závislosť od dávky a trvalé zvýšenie hematokritu, keď bol epoetín alfa podávaný intravenózne aj subkutánne. Podobné rýchlosti rastu hematokritu boli zaznamenané pri podávaní epoetínu alfa obidvom. Navyše dávky epoetínu alfa 75 až 150 IU / kg Ukázalo sa, že týždenne udržuje hematokrit na 36 až 38% počas šiestich mesiacov.
V dvoch predĺžených štúdiách intervalov medzi dávkami lieku EPREX (3 -krát týždenne, raz za týždeň, raz za dva týždne a raz za štyri týždne) niektorí pacienti s dlhšími intervalmi dávkovania neudržali adekvátne hladiny hemoglobínu a splnili stanovené kritériá pre vysadenie lieku (0% raz týždenne, 3,7% raz za 2 týždne a 3,3% v skupinách raz za 4 týždne).
Prospektívna randomizovaná štúdia (CHOIR) hodnotila 1432 anemických pacientov s chronickým zlyhaním obličiek, ktorí nepodstupovali dialýzu. Pacientom bola priradená liečba epoetínom alfa zameraná na udržiavaciu hladinu hemoglobínu 13,5 g / dl (nad odporúčanú hladinu hemoglobínu) alebo 11,3 g / dl. Významná kardiovaskulárna príhoda (smrť, infarkt myokardu, mŕtvica alebo hospitalizácia z dôvodu kongestívneho srdcového zlyhania) , sa vyskytlo u 125 (18%) zo 715 pacientov v skupine s vyšším hemoglobínom v porovnaní s 97 (14%) u 717 pacientov v skupine s nižším hemoglobínom (percento rizika [HR] 1,3, 95%IS: 1,0, 1,7, p = 0,03).
Kumulatívne retrospektívne analýzy klinických štúdií ESA sa vykonali u pacientov s chronickým zlyhaním obličiek (u dialyzovaných a nedialyzovaných pacientov, diabetických a nediabetických pacientov). Bol pozorovaný trend smerom k zvýšenému odhadovanému riziku úmrtnosti na všetky príčiny, kardiovaskulárnych a cerebrovaskulárnych príhod spojených s vyššími kumulatívnymi dávkami ESA bez ohľadu na diabetický alebo dialyzovaný stav pacienta (pozri časť 4.2 a časť 4.4).
Liečba pacientov s anémiou vyvolanou chemoterapiou
Epoetín alfa bol hodnotený v klinických štúdiách u dospelých pacientov s anemickým nádorovým ochorením s lymfoidnými a solídnymi nádormi a u pacientov na rôznych režimoch chemoterapie, vrátane režimov obsahujúcich platinu a neobsahujúcich platinu. V týchto štúdiách sa ukázalo, že epoetín alfa podávaný 3 -krát týždenne a 1 -krát týždenne zvyšuje hemoglobín a znižuje potrebu transfúzií po prvom mesiaci liečby anemických pacientov s rakovinou. V niektorých štúdiách po dvojito zaslepenej fáze nasledovala otvorená fáza, počas ktorej všetci pacienti dostávali epoetín alfa a pozorovalo sa zachovanie účinku.
Dostupné údaje naznačujú, že pacienti s hematologickými malignitami a solídnymi nádormi reagujú na liečbu epoetínom alfa rovnocenne a že pacienti s alebo bez nádorovej infiltrácie kostnej drene reagujú na liečbu epoetínom alfa rovnocenne. Porovnateľná intenzita chemoterapie v skupinách s epoetínom alfa a placebom v štúdiách chemoterapie bola preukázaná podobnou oblasťou pod krivkou času neutrofilov u pacientov liečených epoetínom alfa a placebom, ako aj podobným podielom pacientov v liečených skupinách. s epoetínom alfa a skupinami liečenými placebom, ktorých absolútny počet neutrofilov klesol pod 1 000 a 500 buniek / mcL
V prospektívnej, dvojito zaslepenej, randomizovanej a placebom kontrolovanej štúdii s 375 anemickými pacientmi s nemyeloidnými nádormi, ktorí dostávali chemoterapiu na inom ako platinovom základe, došlo k významnému zníženiu symptómov spojených s anémiou (ako je asténia, únava a znížený krvný tlak) bola zistená. aktivita), merané pomocou nasledujúcich hodnotiacich stupníc: Funkčné hodnotenie rakovinotvornej terapie-anémie (FACT-An) všeobecná stupnica; FACT-Stupnica únavy a lineárna analógová stupnica rakoviny (CLAS).
Dve ďalšie randomizované a placebom kontrolované štúdie vykonané na menšom počte pacientov nepreukázali žiadne zlepšenie parametrov kvality života podľa stupníc EORTC-QLQ-C30 a CLAS.
Prežitie a progresia nádoru sa skúmali v piatich veľkých kontrolovaných štúdiách, do ktorých bolo zapojených celkom 2 833 pacientov, vrátane štyroch dvojito zaslepených placebom kontrolovaných a jednej otvorenej štúdie. Štúdie zaradili pacientov na liečbu chemoterapiou (dve štúdie) a pacientov, u ktorých nebolo použitie ESA indikované: anemickí pacienti s rakovinou nedostávajúci chemoterapiu a pacienti s rakovinou hlavy a krku dostávajúci rádioterapiu. Požadovaná koncentračná hladina rádioterapie. Hemoglobín v dvoch štúdie boli> 13 g / dl; v zostávajúcich troch štúdiách to bolo 12 až 14 g / dl. V otvorenej štúdii nebol žiadny rozdiel v prežití medzi pacientmi liečenými rekombinantným ľudským erytropoetínom a kontrolami. V štyroch kontrolovaných štúdiách bol„pomer nebezpečenstva pre celkové prežitie sa pohyboval od 1,25 do 2,47 v prospech kontrol. Tieto štúdie preukázali nevysvetliteľné štatisticky významné zvýšenie úmrtnosti u pacientov s anémiou rakoviny liečených rekombinantným ľudským erytropoetínom v porovnaní s kontrolami.Celkový výsledok prežitia pacientov liečených rekombinantným ľudským erytropoetínom oproti kontrole nebolo možné uspokojivo vysvetliť rozdielom vo výskyte trombózy a súvisiacich komplikácií.
Analýza na úrovni pacienta bola vykonaná aj u viac ako 13 900 pacientov s rakovinou (chemo-, rádio-, radiochemio- alebo bez terapie), ktorí sa zúčastnili 53 kontrolovaných klinických štúdií s rôznymi epoetínmi. Metaanalýza údajov o celkovom prežití naznačila odhad presného pomeru rizika 1,06 v prospech kontrol (95% IS: 1,00, 1,12; 53 štúdií a 13933 pacientov), zatiaľ čo u pacientov s rakovinou, ktorí dostávali chemoterapiu, celkové prežitie, pokiaľ ide o pomer rizika, bol 1,04 (95% IS: 0,97, 1,11; 38 štúdií a 10441 pacientov). Metaanalýzy ďalej konzistentne naznačujú významné zvýšené relatívne riziko tromboembolických príhod u pacientov s rakovinou, ktorí dostávajú rekombinantné ľudské erytropoetíny (pozri časť 4.4).
Program autológneho darovania
Účinok epoetínu alfa na uľahčenie autológneho darovania krvi u pacientov s nízkym hematokritom (≤ 39% a bez evidentnej anémie spôsobenej nedostatkom železa) plánovaných na veľkú ortopedickú operáciu bol hodnotený v dvojito placebom kontrolovanej štúdii. Zaslepení u 204 pacientov a jedného -slepá placebom kontrolovaná štúdia s 55 pacientmi.
V dvojito zaslepenej štúdii boli pacienti liečení epoetínom alfa 600 IU / kg alebo placebom intravenózne jedenkrát denne každé 3 alebo 4 dni počas 3 týždňov (celkovo 6 dávok). V priemere boli pacienti liečení epoetínom alfa schopní vopred uložiť podstatne viac jednotiek krvi (4,5 jednotky) ako pacienti liečení placebom (3,0 jednotky).
V jednorazovo zaslepenej štúdii boli pacienti liečení epoetínom alfa 300 IU / kg alebo 600 IU / kg alebo placebom intravenózne jedenkrát denne každé 3 alebo 4 dni počas 3 týždňov (celkovo 6 dávok). Pacienti liečení epoetínom alfa boli tiež schopní vopred uložiť významné ďalšie jednotky krvi (epoetín alfa 300 IU / kg = 4,4 jednotiek; epoetín alfa 600 IU / kg = 4,7 jednotiek) v porovnaní s pacientmi liečenými placebom (2,9 jednotiek).
Terapia epoetínom alfa znížila riziko alogénnej expozície krvi o 50% v porovnaní s pacientmi, ktorí neboli liečení epoetínom alfa.
Veľká voliteľná ortopedická chirurgia
Účinok epoetínu alfa (300 IU / kg alebo 100 IU / kg) na expozíciu alogénnym krvným transfúziám bol hodnotený v dvojito zaslepenej, placebom kontrolovanej klinickej štúdii u dospelých pacientov s nedostatkom železa, ktorí čakajú na operáciu. Elektívny ortopedický výkon bedrového kĺbu alebo chirurgický zákrok na kolene. Epoetín alfa bol podávaný subkutánne počas 10 dní pred operáciou, v deň operácie a štyri dni po operácii. Pacienti boli klasifikovaní podľa východiskového hemoglobínu (≤ 10 g / dl,> 10 až ≤ 13 g / dl a> 13 g / dl).
Epoetín alfa 300 IU / kg významne znížil riziko alogénnych transfúzií u pacientov s hemoglobínom pred liečbou z> 10 na ≤ 13 g / dl. 16% pacientov liečených epoetínom alfa 300 IU / kg, 23% epoetínom alfa 100 IU / kg a 45% s placebom vyžaduje transfúziu.
Otvorená štúdia paralelných skupín u dospelých jedincov s nedostatkom železa s hemoglobínom pred liečbou ≥ 10 až ≤ 13 g / dl, ktorí čakali na ortopedickú operáciu bedra alebo kolena, porovnávala liečbu epoetínom alfa 300 IU / kg subkutánne denne počas 10 dní pred operáciou, deň chirurgického zákroku a štyri dni po chirurgickom zákroku, s liečbou epoetínom alfa 600 IU / kg subkutánne jedenkrát týždenne počas 3 týždňov pred chirurgickým zákrokom a v deň chirurgického zákroku.
Od predbežného ošetrenia po pred chirurgickým zákrokom bol priemerný nárast hemoglobínu v skupine s 600 IU / kg (1,44 g / dl) týždenne dvojnásobný v porovnaní so skupinou s 300 IU / kg denne (0,73 g / dl). Priemerné hladiny hemoglobínu boli v týchto dvoch liečebných skupinách podobné v celom chirurgickom období.
Erytropoetická odpoveď pozorovaná v oboch liečebných skupinách viedla k podobným mieram transfúzií (16% v skupine s 600 IU / kg / týždeň a 20% v skupine s 300 IU / kg / deň)
Pediatrická populácia
Chronické zlyhanie obličiek
Epoetín alfa bol hodnotený v otvorenej, nerandomizovanej, otvorenej dávke v 52-týždňovej klinickej štúdii u pediatrických pacientov s CRF podstupujúcich hemodialýzu. Priemerný vek pacientov zaradených do štúdie bol 11,6 rokov (rozsah 0,5 až - 20,1 roka).
Epoetín alfa bol podávaný intravenózne v dávke 75 IU / kg / týždeň v 2 alebo 3 rozdelených dávkach po dialýze, titrovaných od 75 IU / kg / týždeň v 4-týždňových intervaloch (až do maximálnej dávky 300 IU / kg / týždeň.), aby sa dosiahlo zvýšenie hemoglobínu o 1 g / dl / mesiac. Požadovaná hladina hemoglobínu bola 9,6 až 11,2 g / dl. Cieľovú hladinu hemoglobínu dosiahlo 81 percent pacientov. Medián času do cieľa bol 11 týždňov, stredná dávka do cieľa bola 150 IU / kg / týždeň. Z pacientov, ktorí dosiahli cieľ, 90% tak urobilo pri dávkovacom režime 3 -krát týždenne.
Po 52 týždňoch zostalo v štúdii 57% pacientov, ktorí dostávali priemernú dávku 200 IU / kg / týždeň.
05.2 Farmakokinetické vlastnosti
Absorpcia
Po subkutánnom podaní sérové hladiny epoetínu alfa vrcholia medzi 12 a 18 hodinami po podaní. Po podaní viacerých týždenných dávok 600 IU / kg podávaných subkutánne nedošlo k akumulácii.
Absolútna biologická dostupnosť subkutánne injekčne podávaného epoetínu alfa je u zdravých jedincov približne 20%.
Distribúcia
Priemerný distribučný objem je 49,3 ml / kg po intravenóznom podaní 50 a 100 IU / kg u zdravých jedincov. Po intravenóznom podaní epoetínu alfa subjektom s chronickým zlyhaním obličiek bol distribučný objem v rozmedzí od 57 do 107 ml / kg po jednorazovom podaní (12 IU / kg) do 42 až 64 ml / kg po podaní viacerých dávok (48 až 192 IU) / kg). V dôsledku toho je distribučný objem o niečo väčší ako objem plazmy.
Vylúčenie
Polčas epoetínu alfa po intravenóznom podaní viacnásobných dávok je u zdravých jedincov približne 4 hodiny. Polčas po subkutánnom podaní sa odhaduje u zdravých osôb približne na 24 hodín.
Priemerná hodnota CL / F pre režimy 150 IU / kg 3 -krát týždenne a 40 000 IU jedenkrát týždenne u zdravých jedincov bola 31,2, respektíve 12,6 ml / h / kg. Priemerná hodnota CL / F pre režimy 150 IU / kg 3 -krát týždenne a 40 000 IU jedenkrát týždenne u anemických subjektov s rakovinou bola 45,8, respektíve 11,3 ml / h / kg. U väčšiny anemických pacientov s rakovinou, ktorí dostávali cyklickú chemoterapiu, bola CL / F nižšia po subkutánnych dávkach 40 000 IU raz týždenne a 150 IU / kg 3 -krát týždenne v porovnaní s hodnotami pre zdravé subjekty.
Linearita / nelinearita
U zdravých jedincov bolo po intravenóznom podaní 150 a 300 IU / kg, 3 -krát týždenne, pozorované na dávke úmerné zvýšenie sérových koncentrácií epoetínu alfa. Jednorazové subkutánne dávky epoetínu alfa 300-2 400 IU / kg viedli k lineárnemu vzťahu medzi priemernou Cmax a dávkou a medzi priemernou AUC a dávkou. Bol pozorovaný inverzný vzťah medzi klírenszrejmé a dávka u zdravých jedincov.
V štúdiách skúmajúcich predĺženie intervalu medzi dávkami (40 000 IU jedenkrát týždenne a 80 000, 100 000 a 120 000 IU dvakrát týždenne) bol pozorovaný lineárny, ale nie dávkovo proporcionálny vzťah medzi priemernou Cmax a dávkou el „Priemerná AUC a dávka v rovnovážnom stave. .
Farmakokinetický / farmakodynamický vzťah
Epoetín alfa vykazuje dávkovo závislý účinok na hematologické parametre, ktorý je nezávislý od spôsobu podania.
Pediatrická populácia
Polčas približne 6,2-8,7 hodiny po viacnásobnom intravenóznom podaní epoetínu alfa bol hlásený u pediatrických pacientov s chronickým zlyhaním obličiek. Farmakokinetický profil epoetínu alfa u detí a dospievajúcich sa zdá byť podobný ako u dospelých.
Zlyhanie obličiek
U pacientov s chronickým zlyhaním obličiek je polčas epoetínu alfa podávaného intravenózne o niečo dlhší, približne 5 hodín, v porovnaní so zdravými subjektmi.
05.3 Predklinické údaje o bezpečnosti
V toxikologických štúdiách s opakovanou dávkou u psov a potkanov, ale nie u opíc, bola liečba epoetínom alfa spojená so subklinickým stavom fibrózy kostnej drene. Fibróza kostnej drene je známou komplikáciou chronického zlyhania obličiek u ľudí a môže súvisieť so sekundárnou hyperparatyreózou alebo môže byť spôsobená neznámymi faktormi.V štúdii na hemodialyzovaných pacientoch liečených epoetínom alfa počas 3 rokov nebol výskyt fibrózy kostnej drene vyšší ako v skupine pacientov na kontrolnej dialýze neliečených epoetínom alfa.
Epoetín alfa neindukuje génové mutácie v baktériách (Amesov test), chromozomálnu aberáciu v cicavčích bunkách, mikrojadrách u myší ani génovú mutáciu v lokuse HGPRT.
Dlhodobé štúdie karcinogenity neboli vykonané. Konfliktné výsledky v literatúre na základe údajov in vitro zo vzoriek ľudských nádorov naznačujú, že erytropoetíny môžu hrať úlohu v proliferácii nádorov, čo má v klinickej praxi neistý význam.
V bunkových kultúrach buniek ľudskej kostnej drene epoetín alfa špecificky stimuluje erytropoézu a nezahŕňa leukopoézu.Na bunkách kostnej drene nebola pozorovaná žiadna cytotoxická aktivita epoetínu alfa.
V štúdiách na zvieratách sa ukázalo, že epoetín alfa znižuje telesnú hmotnosť plodu, spomaľuje osifikáciu a zvyšuje úmrtnosť plodu, ak sa podáva v týždenných dávkach približne 20 -násobku odporúčanej týždennej dávky u ľudí. Tieto zmeny sa považujú za sekundárne k poklesu telesnej hmotnosti matky a význam pre ľudí pri terapeutických dávkach nie je známy.
06.0 FARMACEUTICKÉ INFORMÁCIE
06.1 Pomocné látky
Polysorbát 80
Glycín
Voda na injekciu.
Dihydrát hydrogenfosforečnanu sodného
Dvojsýtny dihydrát fosforečnanu sodného
Chlorid sodný
06.2 Nekompatibilita
Pretože neexistujú štúdie kompatibility, liek sa nesmie miešať s inými liekmi.
06.3 Obdobie platnosti
18 mesiacov.
06.4 Špeciálne opatrenia na uchovávanie
Uchovávajte v chladničke (2 ° C - 8 ° C). Tento teplotný rozsah musí byť zaistený až do doby podania pacientovi.
Uchovávajte v pôvodnom obale na ochranu pred svetlom.
Neuchovávajte v mrazničke ani netraste.
Na ambulantné použitie sa liek môže vyberať z chladničky bez výmeny maximálne na 3 dni pri teplote nepresahujúcej 25 ° C. Ak sa liek nepoužije do konca tohto obdobia, musí sa zlikvidovať.
06.5 Charakter vnútorného obalu a obsahu balenia
0,3 ml (3 000 IU) injekčný roztok v naplnenej injekčnej striekačke (sklo typu I) s piestom (guma potiahnutá teflónom) a ihlou s puzdrom (guma s polypropylénovým povlakom) a bezpečnostným zariadením na ihlu PROTECS (polykarbonát) pripevneným k injekčnej striekačke - balenie po 1.
0,4 ml (4 000 IU) v naplnenej injekčnej striekačke (sklo typu I) s piestom (guma potiahnutá teflónom) a ihlou s puzdrom (guma s polypropylénovým povlakom) a poistkou na ihlu PROTECS (polykarbonát) pripevnenou k injekčnej striekačke-balenie 1.
0,5 ml (5 000 IU) injekčný roztok v naplnenej injekčnej striekačke (sklo typu I) s piestom (teflónovou vrstvou potiahnutou gumou) a ihlou s puzdrom (guma s polypropylénovým povlakom) a bezpečnostným zariadením ihly PROTECS (polykarbonát) pripevneným k injekčnej striekačke - balenie po 1.
0,6 ml (6 000 IU) injekčný roztok v naplnenej injekčnej striekačke (sklo typu I) s piestom (teflónovou vrstvou potiahnutou gumou) a ihlou s puzdrom (guma s polypropylénovým povlakom) a bezpečnostným zariadením ihly PROTECS (polykarbonát) pripevneným k injekčnej striekačke - balenie po 1.
0,8 ml (7 000 IU) injekčný roztok v naplnenej injekčnej striekačke (sklo typu I) s piestom (teflónovou vrstvou potiahnutou gumou) a ihlou s puzdrom (guma s polypropylénovým povlakom) a bezpečnostným zariadením ihly PROTECS (polykarbonát) pripevneným k injekčnej striekačke - balenie po 1.
1,0 ml (10 000 IU) injekčný roztok v naplnenej injekčnej striekačke (sklo typu I) s piestom (guma potiahnutá teflónom) a ihlou s puzdrom (guma s polypropylénovým poťahom) a poistkou na ihlu PROTECS (polykarbonát) pripevnenou k injekčnej striekačke - balenie po 1.
06.6 Návod na použitie a zaobchádzanie
Výrobok sa nesmie použiť a musí sa zlikvidovať:
• Ak je tesnenie poškodené;
• Ak je roztok zafarbený alebo v prítomnosti častíc;
• Ak dôjde k zamrznutiu alebo existuje podozrenie na neho;
• Ak dôjde k poruche chladničky.
Jednorazový výrobok. Po odstránení nechceného množstva roztoku zo striekačky nepodávajte viac ako jednu dávku na injekčnú striekačku. Pozri časť 3. Ako používať EPREX (návod na injekciu) v písomnej informácii pre používateľov.
Naplnené injekčné striekačky sú vybavené bezpečnostným zariadením na ihly PROTECS, aby sa zabránilo riziku prilepenia ihly. Písomná informácia pre používateľov obsahuje všetky informácie o použití a manipulácii s naplnenými injekčnými striekačkami s bezpečnostným zariadením. Ihla PROTECS.
Nepoužitý liek a odpad z tohto lieku musí byť zlikvidovaný v súlade s miestnymi predpismi.
07.0 DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Janssen -Cilag SpA, cez M.Buonarroti, 23. - 20093 Cologno Monzese (MI)
08.0 REGISTRAČNÉ ČÍSLO
027015167 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka s 3 000 IU / 0,3 ml
027015179 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka so 4 000 IU / 0,4ML
027015231 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka s 5 000 IU / 0,5 ml
027015243 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka s 6 000 IU / 0,6ML
027015268 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka s 8 000 IU / 0,8ML
027015181 - „10 000 IU / ML injekčný roztok v naplnenej injekčnej striekačke“ 1 injekčná striekačka s 10 000 IU / 1ML
09.0 DÁTUM PRVEJ REGISTRÁCIE ALEBO OBNOVENIA REGISTRÁCIE
Máj 1989
Obnovenie AIC: 4. augusta 2008
10.0 DÁTUM REVÍZIE TEXTU
08/2015











.jpg)






-cos-cause-e-disturbi-associati.jpg)