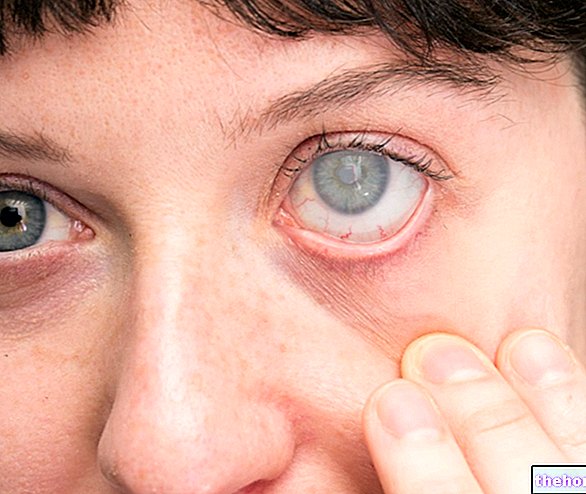
Ako je známe, červené krvinky (RBC) transportujú kyslík do tkanív a pri vytrvalostných športoch, ako je cyklistika, beh na lyžiach atď., Sú požiadavky na kyslík veľmi vysoké.
Už nejaký čas sa preto skúmajú stratégie na zvýšenie produkcie červených krviniek s cieľom zlepšiť športový výkon.
Najnovšia stratégia je založená na úlohe erytropoetínu (EPO) pri stimulácii kostnej drene na produkciu červených krviniek (RBC).
Rekombinantný ľudský EPO (rHuEPO) a príbuzné látky (napr. Darbepoetín) sa používajú ako doping.
EPO má v tele relatívne krátku životnosť, pričom jeho stimulačný účinok môže trvať až dva týždne
d "kyslík1985 Lin a Jacobs klonovali gén erytropoetínu a vyvinuli transfekovanú bunkovú líniu (bunky CHO) schopnú produkovať rekombinantný ľudský erytropoetín
Erytropoéza a hypoxia
Erytropoéza (produkcia nových červených krviniek) je riadená vysoko citlivým systémom spätnej väzby, v ktorom senzor na úrovni obličiek sníma zmeny v dodávke kyslíka.
Mechanizmus je založený na prítomnosti heterodimerického transkripčného faktora (faktor navoditeľný hypoxiou, HIF-1) (HIF-1α a HIF-1β), ktorý zvyšuje expresiu génu pre erytropoetín.
HIF-1a je nestabilný v prítomnosti kyslíka a je rýchlo degradovaný prolylhydroxylázou za prispenia von Hippel-Lindau proteínu.
Počas hypoxie je propylhydroxyláza neaktívna, v dôsledku čoho sa HIF-1a akumuluje aktiváciou expresie erytropoetínu, ktorá stimuluje rýchlu expanziu progenitorov erytroidov.
(ale prvých 27 je oddelených počas sekrécie).
Produkujú ho hlavne peritubulárne intersticiálne bunky obličiek pod kontrolou génu umiestneného na chromozóme 7.
Po sekrécii sa erytropoetín v krvotvornom tkanive (kostná dreň) viaže na receptor (EPO-R) umiestnený na povrchu progenitorov erytroidov a je internalizovaný.
V prítomnosti anémie alebo hypoxémie sa syntéza EPO rýchlo zvyšuje viac ako 100 -krát a následne zvyšuje prežitie, proliferáciu a dozrievanie progenitorových buniek kostnej drene aj prostredníctvom inhibície apoptózy (programovaná bunková smrť).
Normálne hladiny EPO v krvi sú asi 2 až 25 mU / ml, ale v reakcii na hypoxiu sa môžu zvýšiť 100 až 1 000-násobne.
Mechanizmus kyslíkového senzora vedie k prerušeniu produkcie EPO, keď sa počet červených krviniek a / alebo prísun kyslíka do tkanív vráti do rovnováhy
Mechanizmus spätnej väzby zaisťuje adekvátnu produkciu červených krviniek na prevenciu anémie a tkanivovej hypoxie, ale nie príliš vysokú na to, aby viedla k polycytémii s nadmernou viskozitou krvi a následnými kardiovaskulárnymi rizikami.
Nadprodukcia EPO vedúca k polycytémii (sekundárne je možné ju rozlíšiť od polycytémie vera alebo primárnej: myeloproliferatívnej poruchy, kde klony progenitorových buniek nezávislé od EPO proliferujú so zvýšením počtu červených krviniek, granulocytov a krvných doštičiek) môžu byť dôsledkom srdcových alebo respiračných chorôb, z nadmorskej výšky , z prekážok prietoku krvi do miesta výroby EPO, z nádorov produkujúcich EPO.
Pri sekundárnej polycytémii sú hladiny EPO spravidla vysoké, ale môžu byť aj normálne kvôli zvýšeniu jeho obratu.
Je známe, že genetické rozdiely existujúce medzi športovcami môžu byť prvkom na základe rôznych výkonnostných kapacít.
Medzi možnými genetickými rozdielmi sa niektoré môžu týkať erytropoézy všeobecne a konkrétne erytropoetínu.
Príkladom je príbeh fínskeho bežca na lyžiach Eera Mäntyranta, dvojnásobného zlatého medailistu na olympijských hrách 1964 v Innsbrucku.
Narodil sa s génovou mutáciou Epo (vyjadrenou na úrovni receptorov), ktorá zvýšila jeho kapacitu kyslíka v červených krvinkách o 25-50%.
Tento parafyziologický stav je možné reprodukovať génovou manipuláciou.
Počet EPO receptorov sa líši v rôznych bunkách erytrocytovej línie. Maximum sa vyskytuje v CFU-E, počet klesá s postupom diferenciácie a dozrievania erytrocytových buniek. EPO.
Receptory EPO boli tiež identifikované na myocytoch, endotelových bunkách, CNS, vaječníkoch a semenníkoch.
Predpokladá sa, že EPO hrá fyziologickú úlohu vo vývoji srdca a mozgu.
EPO chráni srdcové a nervové tkanivá pred zápalom a ischemickým poškodením: priamou stimuláciou nervových a srdcových buniek a nepriamo mobilizáciou endotelových progenitorových buniek, čím podporuje neo-vaskularizáciu.
) vzhľadom na fyziologický EPO, ktoré sa však odrážajú v chemickom a fyzikálnom správaní molekuly, napríklad existujú rozdiely v elektrickom náboji.Na ergogénne účely sa rHuEPO používa na injekčné podávanie každé 2-3 dni, počas 3-4 týždňov, spojené s prípravkami železa. V skutočnosti je pri stimulácii erytropoetínom nevyhnutné, aby bol hemoglobín syntetizovaný u športovcov oveľa vyššou rýchlosťou, než je obvyklé, a to si vyžaduje adekvátny prísun železa na udržanie erytropoetickej účinnosti. Polčas i.v. 8,5 hodiny.
Akonáhle je dosiahnutá udržiavacia fáza, príjem môže prebiehať v nižších dávkach, ktoré je ťažšie identifikovať pri dopingových kontrolách.
Darbepoietin
Stabilnejší ako EPO, s dlhším polčasom (i.v. 25,3 hodiny) a vyššou účinnosťou; je ľahšie identifikovateľný vďaka svojim štrukturálnym vlastnostiam odlišným od endogénneho humánneho produktu a vďaka jeho nižšiemu klírensu
Terapeutické použitie erytropoetínu (epoetín; Eprex®, Globuren®, Neorecormon®; darbepoetin: Aranesp®, Nespo®)
- Anémia pri chronickom zlyhaní obličiek
- Anémia zidovudínu (anti-HIV)
- "Refraktérna" anémia
- Anémia po protinádorovej chemoterapii
- Patologické nedostatky EPO
- Myelóm
- Myelodysplastické syndrómy.
Rýchlo a neustále sa rozvíjajúci výskum erytropoetínu:
Výrobky, ktoré napodobňujú aktivitu EPO
Malé peptidy alebo nepeptidové zlúčeniny, ktoré sa môžu viazať a aktivovať na receptory EPO (Science 1996; 273: 458. Proc Natl Acad Sci USA 1999; 96: 12156)
Nedávno sa napríklad v pokusoch in vitro ukázalo, že hemolymfa priadky morušovej inhibuje apoptózu buniek produkujúcich EPO päťnásobným zvýšením produkcie EPO (Biotechnol Bioeng 2005; 91: 793)
(hematokrit vyjadrený v percentách), hladiny hemoglobínu, počet retikulocytovV cyklistike vedú merania hematokritu nad 50% k pozastaveniu. Hodnoty nad 50% sú podľa MOV podozrivé
Medzinárodná lyžiarska federácia stanovila limit hemoglobínu 18,5 g / dl u mužov a 16,5 g / dl u žien, ak sa zistí pred súťažou, športovec sa nemôže zúčastniť, aby si zachoval zdravie.
Je potrebné zdôrazniť, že hodnoty hematokritu a hemoglobínu sa môžu líšiť od športovca k športovcovi a v reakcii na rovnaké cvičenie. Ideálne je mať hematologický profil každého športovca v priebehu času:
vyšetrovania s cieľom identifikovať používanie EPO sa rozšírili do rôznych športov a očividne aj na olympijské hry
Marco Pantani bol diskvalifikovaný z Tour po Taliansku za hodnotu hematokritu 52%
V roku 2003 mal keňský bežec na stredné trate Bernard Lagat (druhý najlepší čas na 1 500 m) pozitívny test (výskum rHuEPO v moči) na príjem EPO pred majstrovstvami sveta v atletike v Paríži (na ktorých sa nemohol zúčastniť) analýzy ho však zbavili. Tento prípad ukázal potrebu hľadať spoľahlivejšie testy.
Nedávno bola vyvinutá (s dobrými výsledkami) nová priama izoelektrická metóda na odlíšenie exogénneho od endogénneho EPO vo vzorkách moču, vyvinutá vo francúzskom laboratóriu Chatenay-Malabry (Nature 2000; 405: 635; Anal Biochem 2002; 311: 119; Clin Chem. 2003; 49: 901). Exogénny EPO bolo možné identifikovať aj po 3 dňoch od príjmu
(Výskyt 1-30%). Mechanizmus nie je úplne objasnený. EPO má vazokonstrikčný účinok a chronická expozícia spôsobuje odolnosť voči vazodilatačnému účinku oxidu dusnatého. Nakoniec, EPO podporuje rast buniek hladkých svalov ciev s remodeláciou ciev a hypertrofiou, čo môže prispieť k udržanie hypertenzie [Am J Kidney Dis 1999; 33: 821-8]).
Bolesť kostí (nezávažná, prechodná, vysoký výskyt = 40%).
Kŕče (v dôsledku rýchleho zvýšenia viskozity krvi a straty hypoxickej vazodilatácie s následným zvýšením cievneho odporu).
Bolesť hlavy
Tromboembolické javy (PE, MI, mŕtvica), všetky súvisia s hyperviskozitou krvi.
Anémia po liečbe v dôsledku zníženej produkcie endogénneho EPO.
Čistá aplázia červených krviniek (tvorba anti-EPO protilátky?).
Myeloproliferatívne poruchy (štúdie na zvieratách, dlhodobá liečba?).
Poškodenie erytropoetínom ako doping
Údaje o vyššie uvedených nežiaducich reakciách erytropoetínu pochádzajú takmer výlučne z terapeutických ošetrení pacientov so základnými ochoreniami
Neexistujú žiadne štúdie o škodlivosti erytropoetínu používaného ako doping na zdravých športovcoch
Štúdia na športovcoch, ktorým bol podávaný EPO počas 6 týždňov, zistila významné zvýšenie systolického krvného tlaku v reakcii na sub-maximálne cvičenie.
Počet úmrtí medzi belgickými a holandskými cyklistami v rokoch 1987 až 1990 súvisí s používaním EPO (Gambrell a Lombardo. Drogy a doping: doping krvi a rekombinantný ľudský erytropoetín. In: Mellion, M.B. (ed.): Tajomstvo športovej medicíny. Philadelphia: Hanley & Belfus, 1994, s. 130-3)
Nie je zlé myslieť si, že nežiaduce reakcie pozorované u pacientov sa môžu vyskytnúť aj u zdravých športovcov, aj keď s nižším výskytom.