Glykogén je makromolekula (molekulová hmotnosť asi 400 miliónov daltonov) a-glukózy, v ktorej sú hlavne a-1,4 glykozidické väzby a rozvetvenia v pomere 1:10, v dôsledku a-1,6 glykozidových väzieb.
Glykogén predstavuje rezervný materiál a je neustále degradovaný a rekonštituovaný; v celotelovej bunkovej hmote je asi 100 g glykogénu: väčšina z nich je v pečeni, kde je mobilný, a preto ho možno použiť ako rezervu pre iné orgány (glykogén vo svaloch nie je mobilný).
Enzýmy, ktoré katalyzujú degradáciu a syntézu glykogénu, sú všetky v cytoplazme, preto je potrebný regulačný systém, ktorý robí jednu cestu neaktívnou, keď je druhá aktívna: ak je k dispozícii glukóza, tá sa premení na glykogén (anabolizmus), ktorý je rezerva, naopak, ak je pre glukózu vyžadované c ", potom je glykogén degradovaný (katabolizmus).

Enzým, ktorý sa podieľa predovšetkým na štiepení glykogénu, je glykogénfosforyláza; tento enzým je schopný štiepiť glykozidickú väzbu a-1,4 pomocou anorganického ortofosfátu ako lytického činidla: štiepenie prebieha fosforolytickým spôsobom a získa sa 1-fosfát glukózy.
V piatich alebo šiestich jednotkách z bodu vetvenia už enzým glykogénfosforyláza už nemôže pôsobiť, preto sa od glykogénu oddelí a nahradí ho deramifikačný enzým, ktorý je transferáza: v katalytickom mieste tohto enzýmu c "je" histidín, ktorý umožňuje prenos troch sacharidových jednotiek na najbližší glykozidový reťazec (histidín útočí na prvý uhlík molekuly glukózy). Práve spomínaný enzým je glykozyltransferáza; na konci pôsobenia tohto enzýmu zostáva na bočnom reťazci iba jedna glukózová jednotka s prvým uhlíkom viazaným na šiesty uhlík glukózy v hlavnom reťazci. Posledná glukózová jednotka vo vedľajšom reťazci sa uvoľňuje pôsobením „enzým a-1,6 glykozidázu (tento enzým predstavuje druhú časť deramifikačného enzýmu); vzhľadom na to, že vetvy v glykogéne sú v pomere 1:10, úplnou degradáciou makromolekuly získame asi 90% 1-fosfátu glukózy a asi 10% glukóza.
Pôsobenie vyššie uvedených enzýmov umožňuje elimináciu bočného reťazca z molekuly glykogénu; aktivitu týchto enzýmov je možné opakovať, kým nedôjde k úplnej degradácii reťazca.
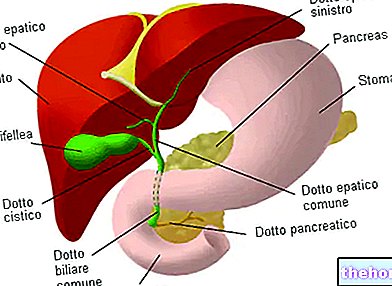
Uvažujme o hepatocyte; glukóza (asimilovaná stravou), pri vstupe do bunky sa premení na 6-fosfát glukózy a tým sa aktivuje. 6-fosfát glukózy, pôsobením fosfoglukomutáza, sa transformuje na glukózo-1-fosfát: ten nie je bezprostredným prekurzorom biosyntézy; pri biosyntéze sa používa aktivovaná forma cukrov, ktorá je reprezentovaná cukrom spojeným s difosfátom: zvyčajne uridyldifosfátom (UDP). 1-fosfát glukózy je potom sa tento metabolit premení na UDP-glukózu, pôsobením glykogén syntáza ktorý je schopný naviazať UDP-glukózu na neredukujúci koniec rastúceho glykogénu: získa sa predĺžený glykogén glukozidovej jednotky a UDP.UDP je konvertovaný nukleozidovým enzýmom difosfokinázou na UTP, ktorý sa vracia do obehu.
K degradácii glykogénu dochádza pôsobením glykogénfosforyláza ktorý uvoľní molekulu glukózy a premení ju na 1-fosfát glukózy. Fosfoglukomutáza následne prevádza 1-fosfát glukózy na 6-fosfát glukózy.
Glykogén sa syntetizuje predovšetkým v pečeni a svaloch: v organizme je 1-1,2 hektogramov glykogénu distribuovaných v celej svalovej hmote.
Glykogén myocytu predstavuje energetickú rezervu iba pre túto bunku, zatiaľ čo glykogén obsiahnutý v pečeni je rezervou aj pre iné tkanivá, to znamená, že môže byť odoslaný ako glukóza do iných buniek.
6-fosfát glukózy získaný vo svaloch degradáciou glykogénu je potom v prípade potreby energie odoslaný na glykolýzu; v pečeni sa glukózo-6-fosfát premieňa na glukózu pôsobením glukóza 6-fosfát fosfatáza (charakteristický enzým hepatocytov) a je transportovaný do krvného obehu.
Glykogénsyntáza a glykogénfosforyláza pôsobia na neredukujúce jednotky glykogénu, takže musí existovať hormonálny signál, ktorý riadi aktiváciu jednej cesty a blokovanie druhej (alebo naopak).
V laboratóriu bolo možné predĺžiť glykogénový reťazec využitím glykogénfosforylázy a použitím 1-fosfátu glukózy vo veľmi vysokej koncentrácii.
Glykogénfosforyláza v bunkách katalyzuje iba degradačnú reakciu, pretože koncentrácie metabolitov posúvajú rovnováhu nasledujúcej reakcie doprava (tj. Smerom k degradácii glykogénu):

Pozrime sa na mechanizmus účinku glykogénfosforylázy: acetalový kyslík (ktorý funguje ako mostík medzi glukózovými jednotkami) sa viaže na vodík fosforylu: reakčný medziprodukt je tvorený karbokationtom (na glukóze, ktorá je všetko " končatiny), na ktoré sa veľmi rýchlo viaže fosforyl (Pi).
Glykogénfosforyláza vyžaduje kofaktor, ktorým je pyridoxalfosfát (táto molekula je tiež kofaktorom pre transaminázy): má čiastočne protonovaný fosforyl (pyridoxalfosfát je obklopený hydrofóbnym prostredím, ktoré odôvodňuje prítomnosť protónov k nemu viazaných). Fosforyl (Pi) je schopný prenášať protón na glykogén, pretože tento fosforyl potom znova získava protón z čiastočne protonizovaného fosforylu pyridoxalfosfátu. Pravdepodobnosť, že pri fyziologickom pH fosforyl stratí svoj protón a zostane úplne deprotonovaný, je veľmi nízka.
Teraz sa pozrime, ako funguje fosfoglukomutáza. Tento enzým predstavuje v katalytickom mieste zvyšok fosforylovaného serínu; serín poskytuje fosforyl na glukózo-1-fosfát (v polohe šesť): krátkodobo sa tvorí 1,6-bisfosfát glukózy, potom sa serín reposforyluje, pričom sa fosforyl dostane do polohy jedna. Fosfogluco mutáza môže fungovať v oboch smeroch, tj. Premena 1-fosfátu glukózy na 6-fosfát glukózy alebo naopak; ak sa vyrába 6-fosfát glukózy, môže byť odoslaný priamo na glykolýzu, do svalov alebo transformovaný na glukózu v pečeni.
Enzým uridylfosfoglukotransferáza (alebo UDP glukóza pyrofosforyláza) katalyzuje reakciu prenosu glukózy-1-fosfátu na UTP naviazaním na fosforyl a.
Enzým, ktorý je práve popísaný, je pyrofosforyláza: tento názov je spôsobený skutočnosťou, že opačnou reakciou ako práve opísaná je pyrofosforylácia.
UDP glukóza, získaná podľa opisu, je schopná predĺžiť glykogénový reťazec monosacharidovou jednotkou.
Reakciu je možné vyvíjať smerom k tvorbe UDP glukózy elimináciou produktu, ktorým je pyrofosfát; enzým pyrofosfatáza premieňa pyrofosfát na dve molekuly ortofosfátu (hydrolýza anhydridu) a pritom udržuje koncentráciu pyrofosfátu tak nízku, aby bol proces tvorby UDP glukózy termodynamicky výhodný.
Ako už bolo spomenuté, UDP glukóza je vďaka pôsobeniu glykogénsyntázy schopná predĺžiť glykogénový reťazec.
Dôsledky (v pomere 1:10) sú dôsledkom skutočnosti, že keď glykogénový reťazec pozostáva z 20-25 jednotiek, zasahuje vetviaci enzým (s „histidínom na katalytickom mieste“), ktorý je schopný prenášať sériu 7 -8 glykozidických jednotiek ďalej za 5-6 jednotkami: tak sa vytvorí nové rozvetvenie.
Z dôvodov nervového pôvodu alebo ak je potrebná energia kvôli fyzickej námahe, adrenalín sa vylučuje z nadobličiek.
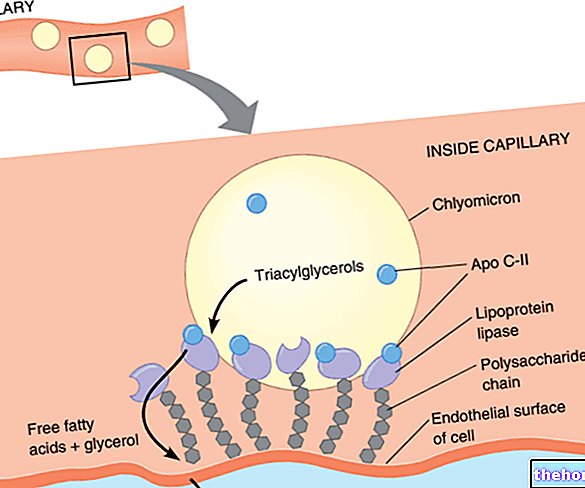
Cieľovými bunkami adrenalínu (a noradrenalínu) sú bunky pečene, svalov a tukového tkaniva (v týchto bunkách dochádza k degradácii triglyceridov a cirkulácii mastných kyselín: v dôsledku toho sa glukóza produkuje v mitochondriách -6 -fosfáte, aby sa odoslané na glykolýzu, zatiaľ čo v adipocytoch sa glukózo-6-fosfát transformuje na glukózu pôsobením enzýmu glukózo-6-fosfátfosfatázy a exportuje sa do tkanív).
Pozrime sa, teraz na spôsoby pôsobenia adrenalínu. Adrenalín sa viaže na receptor umiestnený na bunkovej membráne (myocytov a hepatocytov) a to určuje transláciu signálu zvonku do vnútra bunky. Aktivuje sa proteínkináza, ktorá súčasne pôsobí na systémy, ktoré regulujú syntézu a degradáciu glykogénu:
Glykogénsyntáza existuje v dvoch formách: defosforylovaná (aktívna) forma a fosforylovaná (neaktívna) forma; proteínkináza fosforyluje glykogénsyntázu a blokuje jej pôsobenie.
Glykogénfosforyláza môže existovať v dvoch formách: aktívna forma, v ktorej je prítomný fosforylovaný serín, a neaktívna forma, v ktorej je serín defosforylovaný. Glykogénfosforyláza môže byť aktivovaná enzýmom glykogénfosforylázkináza. Kináza glykogénfosforylázy je aktívna, ak je fosforylovaná, a neaktívna, ak je defosforylovaná; proteínkináza má ako substrát glykogénfosforylázkinázu, to znamená, že je schopná fosforylovať (a teda aktivovať) druhú, ktorá naopak aktivuje glykogénfosforylázu.
Akonáhle sa adrenalínový signál skončí, musí sa tiež skončiť účinok, ktorý má na bunku: enzýmy fosfatázy potom zasahujú do druhov bielkovín.