Účinné látky: valsartan, hydrochlorotiazid
Combisartan 80 mg / 12,5 mg filmom obalené tablety
Combisartan 160 mg / 12,5 mg filmom obalené tablety
Combisartan 160 mg / 25 mg filmom obalené tablety
Combisartan 320 mg / 12,5 mg filmom obalené tablety
Combisartan 320 mg / 25 mg filmom obalené tablety
Indikácie Prečo sa používa Combisartan? Načo to je?
Combisartan filmom obalené tablety obsahujú dve účinné látky nazývané valsartan a hydrochlorotiazid. Obe tieto látky pomáhajú kontrolovať vysoký krvný tlak (hypertenziu).
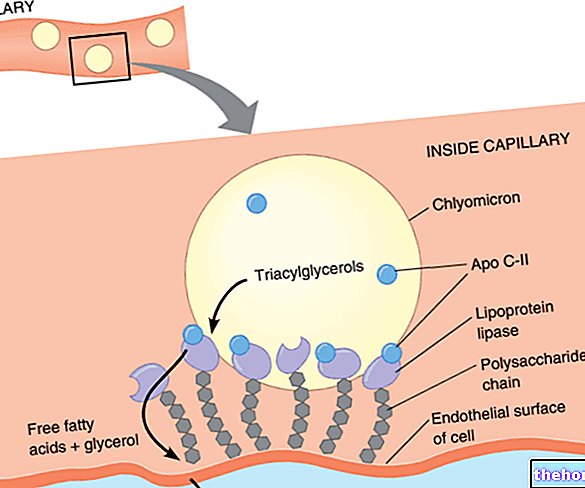
- Valsartan patrí do skupiny liekov známych ako „antagonisty receptora angiotenzínu II“, ktoré pomáhajú kontrolovať vysoký krvný tlak. Angiotenzín II je látka v tele, ktorá spôsobuje zúženie ciev, čo vedie k zvýšeniu tlaku. Valsartan účinkuje tak, že blokuje účinok angiotenzínu II. Výsledkom je, že cievy sa uvoľnia a krvný tlak klesne.
- Hydrochlorotiazid patrí do skupiny liekov nazývaných tiazidové diuretiká.
- Hydrochlorotiazid zvyšuje množstvo vylúčeného moču a tým znižuje krvný tlak.
Combisartan sa používa na liečbu vysokého krvného tlaku, ak krvný tlak nie je dostatočne kontrolovaný jediným liekom.
Keď je krvný tlak vysoký, zvyšuje sa záťaž srdca a tepien. Ak sa nelieči, môže poškodiť cievy mozgu, srdca a obličiek a môže viesť k mŕtvici, zlyhaniu srdca alebo zlyhaniu obličiek. Vysoký krvný tlak zvyšuje riziko srdcového infarktu. Vrátenie krvného tlaku do normálu znižuje riziko vzniku týchto stavov.
Kontraindikácie Kedy sa Combisartan nemá používať
Neužívajte Combisartan:
- ak ste alergický (precitlivený) na valsartan, hydrochlorotiazid, deriváty sulfónamidov (látky chemicky príbuzné hydrochlorotiazidu) alebo na ktorúkoľvek z ďalších zložiek Combisartanu (uvedených v časti 6)
- ak ste tehotná viac ako 3 mesiace (je tiež lepšie vyhnúť sa užívaniu Combisartanu na začiatku tehotenstva - pozri časť tehotenstvo)
- ak máte závažné problémy s pečeňou, deštrukcia malých žlčových kanálikov v pečeni (biliárna cirhóza) vedúca k akumulácii žlče v pečeni (cholestáza)
- ak máte závažné problémy s obličkami
- ak nemôžete močiť (anúria)
- ak ste liečený umelou obličkou
- ak máte hladiny draslíka alebo sodíka v krvi nižšie ako normálne alebo ak máte napriek liečbe hladiny vápnika v krvi vyššie ako normálne
- ak máte dnu
- ak máte cukrovku alebo zhoršenú funkciu obličiek a ste liečený liekom na zníženie krvného tlaku obsahujúcim aliskiren.
Ak sa vás niečo z uvedeného týka, neužívajte tento liek a kontaktujte svojho lekára.
Opatrenia pri používaní Čo potrebujete vedieť predtým, ako užijete Combisartan
Buďte zvlášť opatrný pri Combisartane
- ak užívate lieky šetriace draslík, doplnky draslíka, náhrady soli obsahujúce draslík alebo iné lieky, ktoré zvyšujú hladinu draslíka v krvi, ako je napríklad heparín. Váš lekár vám možno bude musieť pravidelne kontrolovať hladinu draslíka v krvi. krv
- ak máte nízke hladiny draslíka v krvi
- ak máte hnačku alebo silné vracanie
- ak užívate vysoké dávky liekov, ktoré zvyšujú vylučovanie tekutín (diuretiká)
- ak máte vážne problémy so srdcom
- ak máte srdcové zlyhanie alebo ste mali srdcový infarkt. Starostlivo dodržiavajte pokyny lekára o začiatočnej dávke terapie. Váš lekár tiež skontroluje funkciu vašich obličiek.
- ak trpíte zúžením renálnej artérie
- ak ste nedávno dostali novú obličku
- ak trpíte hyperaldosteronizmom, ochorením, pri ktorom nadobličky produkujú príliš veľa hormónu aldosterónu. Ak sa vás to týka, používanie Combisartanu sa neodporúča
- ak máte ochorenie pečene alebo obličiek
- ak ste niekedy mali pri užívaní iných liekov (vrátane ACE inhibítorov) opuch jazyka a tváre spôsobený alergickou reakciou nazývanou angioedém, povedzte to svojmu lekárovi. Ak sa tieto príznaky vyskytnú pri užívaní Combisartanu, okamžite prestaňte užívať Combisartan a už ho nikdy neužívajte. Pozri časť 4, „Možné vedľajšie účinky“
- ak máte horúčku, vyrážku a bolesť kĺbov, ktoré môžu byť znakmi systémového lupus erythematosus (SLE, takzvané autoimunitné ochorenie)
- ak máte cukrovku, dnu, vysokú hladinu cholesterolu alebo triglyceridov v krvi
- ak ste mali alergické reakcie na používanie iných liekov znižujúcich krvný tlak rovnakej triedy (antagonisty receptora angiotenzínu II) alebo ak trpíte alergiou alebo astmou.
- ak máte znížené videnie alebo bolesť očí. Môžu to byť príznaky „zvýšeného vnútroočného tlaku a môžu sa objaviť niekoľko hodín až týždeň po užití Combisartanu. Ak sa nelieči, môže to viesť k trvalej strate zraku. Ak ste v minulosti mali alergiu na penicilíny alebo sulfónamidy. Zvýšené riziko rozvoj tejto poruchy
- môže spôsobiť, že vaša pokožka bude citlivejšia na slnko
- ak užívate niektorý z nasledujúcich liekov používaných na liečbu vysokého krvného tlaku: - „ACE inhibítor“ (napríklad enalapril, lisinopril, ramipril), najmä ak máte problémy s obličkami súvisiace s cukrovkou. - aliskiren
- ak ste liečený inhibítorom ACE spolu s inými liekmi používanými na liečbu srdcového zlyhania, známymi ako antagonisty mineralokortikoidových receptorov (MRA) (napr. spironolaktón, eplerenón) alebo betablokátory (napr. metoprolol).
Váš lekár môže v pravidelných intervaloch kontrolovať funkciu vašich obličiek, krvný tlak a množstvo elektrolytov (napríklad draslíka) v krvi.
Pozri tiež informácie v časti „Neužívajte Combisartan“.
Ak sa vás niečo z uvedeného týka, kontaktujte prosím svojho lekára.
Combisartan sa neodporúča používať u detí a dospievajúcich (mladších ako 18 rokov).
Ak si myslíte, že ste tehotná (alebo ak existuje možnosť, že otehotniete), povedzte to svojmu lekárovi. Combisartan sa neodporúča na začiatku tehotenstva a nesmie sa užívať, ak ste tehotná viac ako 3 mesiace, pretože môže spôsobiť vážne poškodenie vášho dieťaťa, ak sa používa v tomto štádiu (pozri časť Tehotenstvo).
Interakcie Ktoré lieky alebo potraviny môžu meniť účinok Combisartanu
Ak teraz užívate alebo ste v poslednom čase užívali, či práve budete užívať ďalšie lieky, povedzte to svojmu lekárovi alebo lekárnikovi.
Účinok liečby môže byť ovplyvnený, ak je Combisartan užívaný s niektorými inými liekmi.
Možno bude potrebné zmeniť dávku, urobiť iné opatrenia alebo v niektorých prípadoch prestať užívať niektorý z liekov. To platí najmä pre nasledujúce lieky:
- lítium, liek používaný na liečbu niektorých typov psychiatrických porúch
- lieky alebo látky, ktoré môžu zvýšiť množstvo draslíka vo vašej krvi. Patria sem doplnky draslíka alebo náhrady solí obsahujúce draslík, lieky šetriace draslík a heparín
- lieky, ktoré môžu znižovať množstvo draslíka v krvi, ako sú diuretiká (lieky, ktoré zvyšujú elimináciu tekutín), kortikosteroidy, preháňadlá, karboxolón, amfotericín alebo penicilín G.
- niektoré antibiotiká (skupina rifampicín), liek používaný proti odmietnutiu transplantátu (cyklosporín) a antiretrovírusový liek používaný na liečbu infekcií HIV / AIDS (ritonavir). Tieto lieky môžu zvýšiť účinok Combisartanu
- lieky, ktoré môžu vyvolať torsades de pointes (nepravidelný srdcový tep), ako sú antiarytmiká (lieky používané na liečbu srdcových porúch) a niektoré antipsychotiká.
- lieky, ktoré môžu znížiť množstvo sodíka v krvi, ako sú antidepresíva, antipsychotiká, antiepileptiká
- lieky na liečbu dny, ako je alopurinol, probenecid, sulfinpyrazón
- terapeutické doplnky vitamínu D a vápnika,
- lieky používané na liečbu cukrovky (na perorálne použitie, ako je metformín alebo inzulíny)
- iné lieky znižujúce krvný tlak, vrátane metyldopy, ACE inhibítorov (ako je enalapril, lisinopril, atď.) alebo aliskiren (pozri tiež informácie v nadpisoch: „Neužívajte Combisartan“ a „Buďte zvlášť opatrný pri užívaní Combisartanu“).
- lieky, ktoré zvyšujú krvný tlak, ako je norepinefrín a adrenalín
- digoxín alebo iné digitalisové glykozidy (lieky používané na liečbu srdcových problémov)
- lieky, ktoré môžu zvýšiť hladinu cukru v krvi, ako napríklad diazoxid alebo beta blokátory
- cytotoxické lieky (používané na liečbu rakoviny), ako je metotrexát alebo cyklofosfamid
- lieky zmierňujúce bolesť, ako sú nesteroidné protizápalové lieky (NSAID), vrátane selektívnych inhibítorov cyklooxygenázy-2 (Cox-2) a kyseliny acetylsalicylovej> 3 g
- lieky na uvoľnenie svalov, ako je tubokurarín
- anticholinergické lieky (lieky používané na liečbu rôznych ochorení, ako sú gastrointestinálne kŕče, kŕče močového mechúra, astma, kinetóza, svalové kŕče, Parkinsonova choroba a na uľahčenie anestézie)
- amantadín (liek používaný na liečbu Parkinsonovej choroby a tiež na liečbu alebo prevenciu určitých chorôb spôsobených vírusmi)
- cholestyramín a kolestipol (lieky používané hlavne na liečbu vysokých hladín lipidov v krvi)
- cyklosporín, liek používaný pri transplantácii orgánov na prevenciu odmietnutia orgánu
- alkohol, prášky na spanie a anestetiká (lieky s narkotickými alebo úľavovými účinkami používané napríklad počas chirurgického zákroku)
- jódované kontrastné látky (používané na rádiologické vyšetrenia)
Užívanie Combisartanu s jedlom a nápojmi
Combisartan sa môže užívať s jedlom alebo bez jedla. Vyhnite sa pitiu alkoholu, pokiaľ ste sa najskôr neporozprávali so svojim lekárom. Alkohol môže ďalej znižovať krvný tlak a / alebo zvyšovať riziko závratov alebo mdloby.
Upozornenia Je dôležité vedieť, že:
Tehotenstvo a dojčenie
Skôr ako začnete užívať akýkoľvek liek, poraďte sa so svojím lekárom alebo lekárnikom.
- Ak si myslíte, že ste tehotná (alebo ak existuje možnosť, že by ste mohli otehotnieť), musíte to povedať svojmu lekárovi. Váš lekár vám zvyčajne poradí, aby ste prestali užívať Combisartan predtým, ako otehotniete alebo hneď ako začnete vedieť, že ste tehotná a poradí vám, aby ste namiesto Combisartanu užili iný liek. Combisartan sa neodporúča na začiatku tehotenstva a nesmie sa užívať, ak ste tehotná viac ako 3 mesiace, pretože ak sa užíva po treťom mesiaci tehotenstva, môže spôsobiť vážne poškodenie dieťaťa.
- Povedzte svojmu lekárovi, ak dojčíte alebo sa chystáte začať dojčiť
Vedenie vozidla a obsluha strojov
Predtým, ako budete viesť vozidlo, obsluhovať stroje alebo vykonávať iné činnosti, ktoré si vyžadujú koncentráciu, mali by ste poznať svoju reakciu na Combisartan. Tak ako mnohé iné lieky používané na liečbu vysokého krvného tlaku, aj Combisartan môže v zriedkavých prípadoch spôsobiť závrat a ovplyvniť vašu schopnosť koncentrácie.
Pre tých, ktorí vykonávajú športové činnosti: používanie lieku bez terapeutickej potreby predstavuje doping a v každom prípade môže stanoviť pozitívne antidopingové testy.
Dávka, spôsob a čas podávania Ako používať Combisartan: Dávkovanie
Vždy užívajte Combisartan presne tak, ako vám povedal váš lekár. Pomôže vám to dosiahnuť lepšie výsledky a zníži sa riziko vedľajších účinkov. Ak si nie ste istí, poraďte sa so svojím lekárom alebo lekárnikom.
Tí, ktorí majú vysoký krvný tlak, často nevšimnú žiadne známky tohto problému a mnohí sa cítia tak dobre ako obvykle. Z tohto dôvodu je veľmi dôležité, aby ste sa pravidelne navštevovali s lekárom, aj keď sa cítite dobre.
Váš lekár vám presne povie, koľko tabliet Combisartanu máte užiť. Na základe vašej reakcie na liečbu vám lekár môže navrhnúť vyššiu alebo nižšiu dávku.
- Zvyčajná dávka Combisartanu je jedna tableta denne.
- Nemeňte dávku ani neprestaňte užívať tablety bez predchádzajúceho súhlasu lekára.
- Tento liek sa má užívať každý deň v rovnakom čase, zvyčajne ráno.
- Combisartan môžete užívať s jedlom alebo bez jedla.
- Tabletu prehltnite a zapite pohárom vody.
Ak zabudnete užiť Combisartan
Ak zabudnete užiť dávku, vezmite si ju hneď, ako si na to spomeniete. Ak sa však už blíži čas na ďalšiu dávku, vynechanú dávku preskočte.
Neužívajte dvojnásobnú dávku, aby ste nahradili vynechanú dávku.
Ak prestanete užívať Combisartan
Ukončenie liečby Combisartanom môže spôsobiť zhoršenie vášho vysokého krvného tlaku.
Neprestaňte používať svoj liek, pokiaľ vám to nepovie váš lekár.
Ak máte ďalšie otázky týkajúce sa použitia tohto lieku, opýtajte sa svojho lekára alebo lekárnika.
Predávkovanie Čo robiť, ak ste sa predávkovali Combisartanom
V prípade silných závratov a / alebo mdloby je najlepšie ľahnúť si a ihneď kontaktovať lekára.
Ak ste neúmyselne užili príliš veľa tabliet, kontaktujte svojho lekára, lekárnika alebo nemocnicu.
Vedľajšie účinky Aké sú vedľajšie účinky lieku Combisartan
Tak ako všetky lieky, aj Combisartan môže spôsobovať vedľajšie účinky, hoci sa neprejavia u každého.
Tieto vedľajšie účinky sa môžu vyskytnúť s určitou frekvenciou, definovanou nasledovne:
- veľmi časté: postihujú viac ako jedného používateľa z 10
- časté: postihujú 1 až 10 používateľov zo 100
- menej časté: postihujú 1 až 10 používateľov z 1 000
- zriedkavé: postihujú 1 až 10 používateľov z 10 000
- veľmi zriedkavé: postihujú menej ako 1 užívateľa z 10 000
- neznáme: frekvenciu nemožno odhadnúť z dostupných údajov.
Niektoré vedľajšie účinky môžu byť závažné a vyžadujú si okamžitú lekársku pomoc.
Okamžite navštívte lekára, ak máte príznaky angioedému, ako napríklad:
- opuch tváre, jazyka alebo hltana
- ťažkosti s prehĺtaním
- žihľavka a ťažkosti s dýchaním
Ak sa u vás vyskytne ktorýkoľvek z týchto príznakov, prestaňte užívať Combisartan a ihneď kontaktujte svojho lekára (pozri tiež časť 2 „Buďte zvlášť opatrný pri užívaní Combisartanu“).
Ďalšie vedľajšie účinky sú:
Menej časté
- kašeľ
- nízky tlak
- točenie hlavy
- dehydratácia (s príznakmi ako smäd, sucho v ústach a jazyku, zriedkavý moč, tmavý moč, suchá koža)
- svalová bolesť
- únava
- mravčenie alebo znecitlivenie
- rozmazané videnie
- zvuky v ušiach (napr. zvonenie, syčanie)
Veľmi ojedinelý
- závrat
- hnačka
- bolesť kĺbov
Neznáme
- ťažkosti s dýchaním
- znateľné zníženie množstva moču
- nízka hladina sodíka v krvi (ktorá môže v závažných prípadoch spôsobiť únavu, zmätenosť, svalové zášklby a / alebo kŕče)
- nízka hladina draslíka v krvi (niekedy so svalovou slabosťou, svalovými kŕčmi, abnormálnym srdcovým rytmom)
- nízky počet bielych krviniek (s príznakmi, ako je horúčka, kožné infekcie, bolesť hrdla alebo vredy v ústach v dôsledku infekcií, slabosť)
- zvýšená hladina bilirubínu v krvi (ktorá môže v závažných prípadoch spôsobiť zožltnutie pokožky a očí)
- zvýšenie hladín močoviny a kreatinínu v krvi (čo môže naznačovať zlyhanie obličiek)
- zvýšená hladina kyseliny močovej v krvi (ktorá môže v závažných prípadoch spôsobiť dnu)
- synkopa (mdloby)
Nasledujúce vedľajšie účinky boli hlásené pri liekoch obsahujúcich samotný valsartan alebo hydrochlorotiazid:
Valsartan
Menej časté
- pocit točenia hlavy
- bolesť brucha
Neznáme
- pľuzgiere na koži (znak bulóznej dermatitídy)
- vyrážka so svrbením alebo bez svrbenia spolu s niektorými z nasledujúcich prejavov alebo symptómov: horúčka, bolesť kĺbov, bolesť svalov, zdurené lymfatické uzliny a / alebo príznaky podobné chrípke
- vyrážka, červenofialové škvrny, horúčka, svrbenie (príznaky zápalu ciev)
- nízky počet krvných doštičiek v krvi (niekedy s neobvyklým krvácaním alebo podliatinami)
- zvýšená hladina draslíka v krvi (niekedy so svalovými kŕčmi, abnormálnym srdcovým rytmom)
- alergické reakcie (s príznakmi ako je vyrážka, svrbenie, žihľavka, ťažkosti s dýchaním alebo prehĺtaním, závrat)
- opuch hlavne tváre a hrdla, vyrážka, svrbenie
- zvýšenie hodnôt funkcie pečene
- pokles hladín hemoglobínu a percento červených krviniek v krvi (čo môže v závažných prípadoch viesť k anémii)
- zlyhanie obličiek
- nízka hladina sodíka v krvi (ktorá môže v závažných prípadoch spôsobiť únavu, zmätenosť, svalové zášklby a / alebo kŕče)
Hydrochlorotiazid
Velmi bezne
- nízka hladina draslíka v krvi
- zvýšené krvné lipidy
spoločný
- nízka hladina sodíka v krvi
- nízka hladina horčíka v krvi
- vysoká hladina kyseliny močovej v krvi
- svrbivé kožné vyrážky alebo iné druhy vyrážok
- znížená chuť do jedla
- mierna nevoľnosť a vracanie
- závraty, mdloby pri vzpriamenom stoji
- neschopnosť dosiahnuť alebo udržať erekciu
Zriedkavé
- opuch a tvorba pľuzgierov na koži (v dôsledku „zvýšenej citlivosti na slnko)
- vysoká hladina vápnika v krvi
- vysoká hladina cukru v krvi
- cukor v moči
- zhoršenie metabolického stavu cukrovky
- zápcha, hnačka, podráždený žalúdok alebo črevá, poruchy pečene, ktoré sa môžu vyskytnúť so žltou pokožkou alebo očami
- nepravidelný srdcový tep
- bolesť hlavy
- poruchy spánku
- smútok (depresia)
- nízka hladina krvných doštičiek (niekedy s krvácaním alebo podliatinami pod kožou)
- závrat
- mravčenie alebo znecitlivenie
- poruchy videnia
Veľmi ojedinelý
- zápal ciev s príznakmi ako je kožná vyrážka, purpurové červené škvrny, horúčka (vaskulitída)
- vyrážka, svrbenie, žihľavka, ťažkosti s dýchaním alebo prehĺtaním, závrat (reakcie z precitlivenosti)
- závažné kožné stavy spôsobujúce vyrážku, začervenanie kože, pľuzgiere na perách, očiach alebo v ústach, olupovanie kože, horúčka (toxická epidermálna nekrolýza)
- vyrážky na tvári, bolesť kĺbov, svalové poruchy, horúčka (lupus erythematosus)
- silná bolesť v hornej časti žalúdka (pankreatitída)
- ťažkosti s dýchaním s horúčkou, kašľom, sipotom, dýchavičnosťou (ťažkosti s dýchaním vrátane zápalu pľúc a pľúcneho edému)
- horúčka, bolesť hrdla, časté infekcie (agranulocytóza)
- bledá koža, únava, dýchavičnosť, tmavý moč (hemolytická anémia)
- horúčka, bolesť hrdla alebo vredy v ústach v dôsledku infekcií (leukopénia)
- zmätenosť, únava, svalový chvenie alebo kŕče, dýchavičnosť (hypochloremická alkalóza)
Neznáme
- únava, podliatiny a časté infekcie (aplastická anémia)
- závažné zníženie množstva moču (možný znak poruchy obličiek alebo zlyhania obličiek)
- znížené videnie alebo bolesť oka v dôsledku vysokého očného tlaku (možný príznak akútneho glaukómu s úzkym uhlom)
- vyrážka, začervenanie kože, pľuzgiere na perách, očiach alebo v ústach, olupovanie kože, horúčka (možné prejavy multiformného erytému)
- svalový kŕč
- horúčka (pyrexia)
- slabosť (asténia)
Ak začnete pociťovať akýkoľvek vedľajší účinok ako závažný alebo ak spozorujete vedľajšie účinky, ktoré nie sú uvedené v tejto písomnej informácii pre používateľov, povedzte to, prosím, svojmu lekárovi alebo lekárnikovi.
Expirácia a retencia
- Uchovávajte Combisartan mimo dosahu a dohľadu detí.
- Nepoužívajte Combisartan po dátume exspirácie, ktorý je uvedený na štítku. Dátum exspirácie sa vzťahuje na posledný deň v danom mesiaci.
- Uchovávajte pri teplote neprevyšujúcej 30 ° C. Uchovávajte v pôvodnom obale na ochranu pred vlhkosťou.
- Nepoužívajte Combisartan, ak spozorujete, že balenie je poškodené alebo javí známky nedovoleného zaobchádzania.
- Lieky sa nesmú likvidovať odpadovou vodou alebo domovým odpadom. Opýtajte sa svojho lekárnika, ako zlikvidovať lieky, ktoré už nepoužívate. Pomôže to chrániť životné prostredie.
Termín "> Ďalšie informácie
Čo Combisartan obsahuje
- Účinnými látkami sú valsartan a hydrochlorotiazid. Každá filmom obalená tableta obsahuje 80 mg, 160 mg alebo 320 mg valsartanu a 12,5 mg alebo 25 mg hydrochlorotiazidu.
- Jadro tablety obsahuje mikrokryštalickú celulózu, krospovidón, bezvodý koloidný oxid kremičitý, magnéziumstearát.
- Obal tablety obsahuje hypromelózu, makrogol 8000 (iba 80 mg / 12,5 mg a 160 mg / 12,5 mg), makrogol 4000 (iba 160 mg / 25 mg, 320 mg / 12,5 mg a 320 mg / 25) mg), mastenec, červený oxid železitý (E172, okrem 320 mg / 25 mg), žltý oxid železitý (E172, iba 80 mg / 12,5 mg, 160 mg / 12,5 mg a 320 mg / 12,5 mg) mg), čierny oxid železitý (E172, iba 160 mg / 25 mg a 320 mg / 12,5 mg), oxid titaničitý (E171).
Opis toho, ako Combisartan vyzerá a obsah balenia
- Combisartan 80 mg / 12,5 mg filmom obalené tablety sú svetlooranžové, oválne, s vyrazeným „HGH“ na jednej strane a „CG“ na druhej strane alebo „HGH“ iba na jednej strane.
- Combisartan 160 mg / 12,5 mg filmom obalené tablety sú tmavočervené, oválne, s vyrazeným „HHH“ na jednej strane a „CG“ na druhej strane alebo „HHH“ iba na jednej strane.
- Combisartan 160 mg / 25 mg filmom obalené tablety sú hnedé, oválne, s vyrazeným „HXH“ na jednej strane a „NVR“ na druhej strane alebo „HXH“ iba na jednej strane.
- Combisartan 320 mg / 12,5 mg filmom obalené tablety sú ružové, oválne, so skoseným okrajom, s vyrazeným „NVR“ na jednej strane a „HIL“ na druhej strane alebo „HIL“ iba na jednej strane.
- Combisartan 320 mg / 25 mg filmom obalené tablety sú žlté, oválne, s vyrazeným „CTI“ na jednej strane a „NVR“ na druhej strane alebo „CTI“ vyraženým iba na jednej strane.
Tablety Combisartan 80 mg / 12,5 mg sú dostupné v kalendárových blistroch, v baleniach po 14 alebo 28 tabliet.
Tablety Combisartan 160 mg / 12,5 mg, 160 mg / 25 mg, 320 mg / 12,5 mg a 320 mg / 25 mg sú dostupné v kalendárových blistroch, v baleniach po 7 (iba 320 mg / 12,5 mg a 320 mg / 25 mg), 14, 28, 56, 98 alebo 280 tabliet.
K dispozícii sú aj deliteľné jednodávkové blistre v baleniach po 56 x 1 (iba 320 mg / 12,5 a 320 mg / 25 mg), 98 x 1 (okrem 80 mg / 12,5) alebo 280 x 1 (iba 320 mg / 12,5 a 320 mg / 25 mg) tabliet .
Na trh nemusia byť uvedené všetky veľkosti balenia.
Zdrojový leták: AIFA (Talianska agentúra pre lieky). Obsah zverejnený v januári 2016. Súčasné informácie nemusia byť aktuálne.
Aby ste mali prístup k najaktuálnejšej verzii, odporúča sa navštíviť webovú stránku AIFA (Talianska agentúra pre lieky). Vylúčenie zodpovednosti a užitočné informácie.
01.0 NÁZOV LIEKU -
TABLETY COMBISARTAN 160 MG / 12,5 MG potiahnuté filmom
02.0 KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE -
Každá tableta obsahuje 160 mg valsartanu a 12,5 mg hydrochlorotiazidu.
Úplný zoznam pomocných látok, pozri časť 6.1.
03.0 LIEKOVÁ FORMA -
Filmom obalená tableta.
Tmavočervená, oválna tableta s vyrytými písmenami „HHH“ na jednej strane a „CG“ na druhej strane alebo s vyrytými písmenami „HHH“ iba na jednej strane.
04.0 KLINICKÉ INFORMÁCIE -
04.1 Terapeutické indikácie -
Liečba esenciálnej arteriálnej hypertenzie u dospelých.
Combisartan je fixná kombinácia indikovaná u pacientov, ktorých krvný tlak nie je dostatočne kontrolovaný monoterapiou valsartanom alebo hydrochlorotiazidom.
04.2 Dávkovanie a spôsob podávania -
Dávkovanie
Odporúčaná dávka Combisartanu 160 mg / 12,5 mg je jedna filmom obalená tableta jedenkrát denne. Odporúča sa titrácia dávky jednotlivými zložkami. V každom prípade by sa mala vykonať titrácia jednotlivých zložiek na nasledujúcu dávku, aby sa znížilo riziko hypotenzie a iných nežiaducich účinkov.
Ak je to klinicky vhodné, u pacientov, ktorých krvný tlak nie je dostatočne kontrolovaný monoterapiou valsartanom alebo hydrochlorotiazidom, je možné zvážiť priamy prechod z monoterapie na fixnú kombináciu za predpokladu, že sa dodržiava odporúčaná postupnosť titrácie dávky pre jednotlivé zložky.
Klinická odpoveď na Combisartan sa má vyhodnotiť po začatí terapie a ak zostane krvný tlak nekontrolovaný, dávka ktorejkoľvek zložky sa môže zvýšiť až na maximálnu dávku Combisartanu 320 mg / 25 mg.
Antihypertenzívny účinok je v zásade prítomný do 2 týždňov.
U väčšiny pacientov je maximálny účinok pozorovaný do 4 týždňov. U niektorých pacientov však môže byť potrebných 4-8 týždňov liečby. Toto je potrebné vziať do úvahy pri titrácii dávky.
Spôsob podávania
Combisartan sa môže užívať s jedlom alebo bez jedla a má sa zapiť vodou.
Špeciálne populácie
Poškodenie obličiek
U pacientov s miernym až stredne ťažkým poškodením funkcie obličiek (rýchlosť glomerulárnej filtrácie ≥ 30 ml / min) nie je potrebná žiadna úprava dávky. Vzhľadom na hydrochlorotiazidovú zložku je Combisartan kontraindikovaný u pacientov s ťažkým poškodením funkcie obličiek (anúria glomerulárnej filtrácie (pozri časti 4.3, 4.4 a 5.2).
Pečeňová insuficiencia
U pacientov s miernou alebo stredne závažnou poruchou funkcie pečene bez cholestázy by dávka valsartanu nemala prekročiť 80 mg (pozri časť 4.4). U pacientov s miernym až stredne ťažkým poškodením funkcie pečene nie je potrebná úprava dávky hydrochlorotiazidu. Vzhľadom na valsartanovú zložku je Combisartan kontraindikovaný u pacientov s ťažkým poškodením funkcie pečene alebo s biliárnou cirhózou a cholestázou (pozri časti 4.3, 4.4 a 5.2).
Seniori
U starších pacientov nie je potrebná žiadna úprava dávky.
Detských pacientov
Combisartan sa neodporúča používať u detí mladších ako 18 rokov kvôli nedostatku údajov o bezpečnosti a účinnosti.
04.3 Kontraindikácie -
• Precitlivenosť na valsartan, hydrochlorotiazid, iné lieky obsahujúce deriváty sulfónamidov alebo na niektorú z pomocných látok.
• Druhý a tretí trimester gravidity (pozri časti 4.4 a 4.6).
• Závažné poškodenie funkcie pečene, biliárna cirhóza a cholestáza.
• Závažné poškodenie obličiek (klírens kreatinínu
• Refraktérna hypokaliémia, hyponatriémia, hyperkalcémia a symptomatická hyperurikémia.
• Súbežné používanie Combisartanu s liekmi obsahujúcimi aliskiren je kontraindikované u pacientov s diabetes mellitus alebo s poruchou funkcie obličiek (glomerulárna filtrácia GFR
04.4 Špeciálne upozornenia a vhodné opatrenia pri používaní -
Zmeny sérových elektrolytov
Valsartan
Súbežné používanie doplnkov draslíka, draslík šetriacich diuretík, náhrad solí obsahujúcich draslík alebo iných látok, ktoré môžu zvýšiť hladinu draslíka (heparín atď.), Sa neodporúča. Hladinu draslíka v krvi je potrebné náležite kontrolovať.
Hydrochlorotiazid
Počas liečby tiazidovými diuretikami vrátane hydrochlorotiazidu bola hlásená hypokaliémia. Odporúča sa časté monitorovanie sérového draslíka.
Liečba tiazidovými diuretikami, vrátane hydrochlorotiazidu, je spojená s hyponatrémiou a hypochloremickou alkalózou. Tiazidy vrátane hydrochlorotiazidu zvyšujú vylučovanie horčíka močom, a preto môže dôjsť k hypomagneziémii. Zníženej tiazidovými diuretikami, čo môže spôsobiť hyperkalciémiu.
Rovnako ako u všetkých pacientov na diuretickej terapii, má sa vo vhodných intervaloch vykonávať pravidelné monitorovanie sérových elektrolytov.
Pacienti s depléciou sodíka a / alebo objemu
U pacientov užívajúcich tiazidové diuretiká vrátane hydrochlorotiazidu je potrebné sledovať klinické príznaky nerovnováhy tekutín alebo elektrolytov.
U pacientov s veľmi zníženým príjmom sodíka a / alebo objemu, ako sú pacienti, ktorí dostávajú vysoké dávky diuretík, sa v zriedkavých prípadoch môže objaviť symptomatická hypotenzia po začatí liečby Combisartanom. Deplécia sodíka a / alebo objemu sa má najskôr upraviť. Na začiatku liečby Combisartanom .
Pacienti s ťažkým chronickým srdcovým zlyhaním alebo inými stavmi, ktoré stimulujú systém renín-angiotenzín-aldosterón
U pacientov, ktorých funkcia obličiek môže závisieť od aktivity systému renín-angiotenzín-aldosterón (napr. Pacienti s ťažkým kongestívnym srdcovým zlyhaním), bola liečba inhibítormi enzýmu konvertujúceho angiotenzín spojená s oligúriou a / alebo progresívnou azotémiou a v zriedkavých prípadoch akútne zlyhanie obličiek a / alebo smrť. Hodnotenie pacientov so srdcovým zlyhaním alebo po infarkte myokardu by malo vždy zahŕňať vyšetrenie funkcie obličiek. Použitie Combisartanu u pacientov s ťažkým chronickým srdcovým zlyhaním nebolo stanovené. Preto nemožno vylúčiť, že v dôsledku inhibície systému renín-angiotenzín-aldosterónový podanie môže byť sprevádzaný aj poruchou funkcie obličiek. Combisartan sa nemá používať u týchto pacientov.
Stenóza renálnej artérie
Combisartan sa nemá používať ako antihypertenzívum u pacientov s jednostrannou alebo obojstrannou stenózou renálnej artérie alebo stenózou artérie jednej obličky, pretože u týchto pacientov sa môže zvýšiť BUN a sérový kreatinín.
Primárny hyperaldosteronizmus
Pacienti s primárnym aldosteronizmom by nemali byť liečení Combisartanom, pretože ich systém renín-angiotenzín nie je aktívny.
Stenóza aortálnej a mitrálnej chlopne, obštrukčná hypertrofická kardiomyopatia
Rovnako ako u všetkých ostatných vazodilatancií je potrebná osobitná opatrnosť u pacientov trpiacich aortálnou alebo mitrálnou stenózou alebo obštrukčnou hypertrofickou kardiomyopatiou.
Porucha funkcie obličiek
U pacientov s poruchou funkcie obličiek s klírensom kreatinínu ≥ 30 ml / min nie je potrebná žiadna úprava dávky (pozri časť 4.2). Keď sa Combisartan používa u pacientov s poruchou funkcie obličiek, odporúča sa pravidelné monitorovanie hladín draslíka, kreatinínu a kyseliny močovej v sére.
Transplantácia obličky
Doteraz nie sú skúsenosti s bezpečným používaním Combisartanu u pacientov, ktorí nedávno podstúpili transplantáciu obličky.
Poškodenie funkcie pečene
U pacientov s miernym alebo stredne ťažkým poškodením funkcie pečene bez cholestázy sa má Combisartan používať s opatrnosťou (pozri časti 4.2 a 5.2). Tiazidové diuretiká sa majú používať opatrne u pacientov s poruchou funkcie pečene alebo progresívnym ochorením pečene, pretože minimálne zmeny v rovnováhe tekutín a elektrolytov môžu spôsobiť hepatálnu kómu.
Predchádzajúce epizódy angioedému
U pacientov liečených valsartanom boli hlásené epizódy angioedému so zvýšením hrtana a hlasiviek, ktoré majú za následok obštrukciu dýchacích ciest a / alebo opuch tváre, pier, hltana a / alebo jazyka; niektorí z týchto pacientov mali v minulosti epizódy angioedému s inými liekmi, vrátane ACE inhibítorov. U pacientov, u ktorých sa vyvinie angioedém, sa má liečba Combisartanom okamžite ukončiť a nesmie sa znova začať (pozri časť 4.8).
Systémový lupus erythematosus
Ukázalo sa, že tiazidové diuretiká vrátane hydrochlorotiazidu zhoršujú alebo aktivujú systémový lupus erythematosus.
Iné metabolické poruchy
Tiazidové diuretiká, vrátane hydrochlorotiazidu, môžu narušiť toleranciu glukózy a zvýšiť hladiny cholesterolu, triglyceridov a kyseliny močovej v sére. U diabetických pacientov môže byť potrebná úprava dávky inzulínu alebo perorálnych hypoglykemických liekov.
Tiazidy môžu znížiť vylučovanie vápnika močom a spôsobiť mierny a prerušovaný nárast vápnika v sére bez známych porúch metabolizmu vápnika. Výrazná hyperkalcémia môže byť dôkazom základnej hyperparatyreózy. Pred vykonaním testov funkcie prištítnych teliesok. Liečba tiazidmi sa má ukončiť.
Fotosenzitivita
Počas liečby tiazidovými diuretikami boli hlásené prípady fotosenzitívnych reakcií (pozri časť 4.8). Ak sa vyskytnú fotosenzitívne reakcie, odporúča sa prerušiť liečbu. Ak sa považuje za nevyhnutné pokračovať v podávaní diuretík, odporúča sa chrániť časti vystavené slnku alebo umelým lúčom UVA.
Tehotenstvo
Terapia antagonistami receptora angiotenzínu II (AIIRA) sa nemá začať počas gravidity. U pacientok plánujúcich graviditu sa má použiť alternatívna antihypertenzívna liečba s preukázaným bezpečnostným profilom na použitie v gravidite. Pokiaľ sa pokračovanie terapie AIIRA nepovažuje za nevyhnutné. Keď je diagnostikované tehotenstvo, liečba AIIRA sa má ihneď ukončiť a ak je to vhodné, má sa začať alternatívna liečba (pozri časti 4.3 a 4.6).
Generál
Zvláštna opatrnosť je potrebná u pacientov, ktorí mali v minulosti reakcie z precitlivenosti na iné antagonisty receptora angiotenzínu II. Reakcie z precitlivenosti na hydrochlorotiazid sú pravdepodobnejšie u pacientov s alergiou a astmou.
Akútny glaukóm s uzavretým uhlom
Hydrochlorotiazid, sulfónamid, je spájaný s idiosynkratickou reakciou, ktorá má za následok závažnú prechodnú krátkozrakosť a akútny glaukóm s úzkym uhlom. Medzi príznaky patrí akútny nástup zníženej zrakovej ostrosti alebo bolesti očí a zvyčajne sa prejavia do niekoľkých hodín až jedného týždňa po začiatku liečby. Ak sú ponechané neliečený akútny glaukóm s uzavretým uhlom môže spôsobiť trvalú stratu zraku.
Primárnou liečbou je „čo najrýchlejšie prerušenie podávania hydrochlorotiazidu. Ak vnútroočný tlak zostane nekontrolovaný, môže byť potrebná rýchla lekárska alebo chirurgická intervencia. Rizikové faktory vzniku akútneho glaukómu s úzkym uhlom môžu zahŕňať alergiu na sulfónamid alebo penicilín v anamnéze.
Dvojitá blokáda systému renín-angiotenzín-aldosterón (RAAS)
Existuje dôkaz, že súbežné používanie inhibítorov ACE, blokátorov receptorov angiotenzínu II alebo aliskirenu zvyšuje riziko hypotenzie, hyperkaliémie a zníženej funkcie obličiek (vrátane akútneho zlyhania obličiek). Dvojitá blokáda RAAS kombinovaným použitím ACE inhibítorov, blokátorov receptorov angiotenzínu II alebo aliskirenu sa preto neodporúča (pozri časti 4.5 a 5.1).
Ak je dvojbloková terapia považovaná za absolútne nevyhnutnú, mala by byť vykonaná iba pod dohľadom odborníka a za dôsledného a častého monitorovania funkcie obličiek, elektrolytov a krvného tlaku.
Inhibítory ACE a antagonisty receptora angiotenzínu II by sa nemali používať súbežne u pacientov s diabetickou nefropatiou.
04.5 Interakcie s inými liekmi a iné formy interakcie -
Interakcie súvisiace s valsartanom aj hydrochlorotiazidom
Súbežné použitie sa neodporúča
Lítium
Pri súbežnom podávaní lítia s ACE inhibítormi, antagonistami receptora angiotenzínu II alebo tiazidmi vrátane hydrochlorotiazidu bolo hlásené reverzibilné zvýšenie sérových koncentrácií a toxicity lítia. Pretože renálny klírens lítia je tiazidmi znížený, riziko toxicity lítia sa môže pri použití Combisartanu pravdepodobne ešte zvýšiť. Ak je použitie tejto kombinácie nevyhnutné, odporúča sa starostlivé monitorovanie hladín lítia v sére.
Súbežné používanie vyžadujúce opatrnosť
Iné antihypertenzíva
Combisartan môže zosilniť účinky iných liekov s antihypertenzívnymi vlastnosťami (napr. Guanetidín, metyldopa, vazodilatátory, ACE inhibítory, antagonisty receptora angiotenzínu, beta-blokátory, blokátory kalciových kanálov a renínové inhibítory).
Presorické amíny (napr. adrenalín, noradrenalín)
Je možné zníženie reakcie na presorické amíny. Klinický význam tohto účinku je neistý a nepostačuje na vylúčenie ich použitia.
Nesteroidné protizápalové lieky (NSAID), vrátane selektívnych inhibítorov COX-2, kyseliny acetylsalicylovej (> 3 g / deň) a neselektívnych NSAID
Pri súbežnom podávaní môžu NSAID oslabiť antihypertenzívny účinok antagonistov angiotenzínu II a hydrochlorotiazidu. Súčasné používanie Combisartanu a NSAID môže okrem toho viesť k zhoršeniu funkcie obličiek a zvýšeniu draslíka v sére. Na začiatku liečby sa preto odporúča skontrolovať funkciu obličiek a adekvátnu hydratáciu pacienta.
Interakcie súvisiace s valsartanom
Dvojitá blokáda systému renín-angiotenzín-aldosterón (RAAS) s ARB, ACEI alebo aliskirenom
Údaje z klinických štúdií ukázali, že duálna blokáda systému renín-angiotenzín-aldosterón (RAAS) kombinovaným používaním inhibítorov ACE, blokátorov receptorov angiotenzínu II alebo aliskirenu je spojená s vyššou frekvenciou nežiaducich účinkov, ako je hypotenzia, hyperkaliémia a zníženie funkcia obličiek (vrátane akútneho zlyhania obličiek) v porovnaní s použitím jediného liečiva aktívneho v systéme RAAS (pozri časti 4.3, 4.4 a 5.1).
Súbežné použitie sa neodporúča
Draslík šetriace diuretiká, doplnky draslíka, náhrady kuchynskej soli s obsahom draslíka a ďalšie látky, ktoré môžu zvýšiť hladinu draslíka.
Ak je použitie kombinácie valsartanu s liekom, ktorý mení hladiny draslíka, nevyhnutné, odporúča sa monitorovať plazmatické hladiny draslíka.
Dopravníky
Údaje in vitro naznačujú, že valsartan je substrátom transportérov absorpcie v pečeni OATP1B1 / OATP1B3 a transportéra hepatálnych efluxov MRP2. Klinický význam tohto pozorovania nie je známy. Súbežné podávanie inhibítorov transportéra vychytávania (napr. Rifampicín, cyklosporín) alebo efluxného transportéra (napr. Ritonavir) môže zvýšiť systémovú expozíciu valsartanu. Osobitnú pozornosť treba venovať začatiu alebo ukončeniu súbežnej liečby týmito liekmi.
Žiadna interakcia
V interakčných štúdiách zahŕňajúcich valsartan neboli zistené žiadne klinicky významné interakcie s valsartanom alebo s niektorým z nasledujúcich liekov: cimetidín, warfarín, furosemid, digoxín, atenolol, indometacín, hydrochlorotiazid, amlodipín, glibenklamid. Digoxín a indometacín môžu interagovať s hydrochlorotiazidovou zložkou Combisartanu (pozri interakcie súvisiace s hydrochlorotiazidom).
Interakcie súvisiace s hydrochlorotiazidom
Súbežné používanie vyžadujúce opatrnosť
Lieky ovplyvňujúce hladinu draslíka v sére.
Hypokaliemický účinok hydrochlorotiazidu je možné zvýšiť súbežným podávaním kaliuretických diuretík, kortikosteroidov, laxatív, ACTH, amfotericínu, karbenoxolónu, penicilínu G, kyseliny salicylovej a jej derivátov.
Ak majú byť tieto lieky predpísané s kombináciou valsartan-hydrochlorotiazid, odporúča sa monitorovanie plazmatických hladín draslíka (pozri časť 4.4).
Lieky, ktoré môžu vyvolať torsades de pointes
Vzhľadom na riziko hypokaliémie sa má hydrochlorotiazid podávať s opatrnosťou v kombinácii s liekmi, ktoré môžu indukovať torsades de pointes, najmä antiarytmikami triedy Ia a triedy III a niektorými antipsychotikami.
Lieky ovplyvňujúce hladinu sodíka v sére
Hyponatremický účinok diuretík môže byť zosilnený súbežným podávaním určitých liekov, ako sú antidepresíva, antipsychotiká, antiepileptiká, atď. Pri dlhodobom podávaní týchto liekov sa odporúča opatrnosť.
Digitalisové glykozidy
Ako nežiaduce účinky sa môže vyskytnúť hypokaliémia alebo hypomagneziémia vyvolaná tiazidmi, ktoré podporujú nástup srdcových arytmií vyvolaných digitálisom (pozri časť 4.4).
Soli vápnika a vitamínu D.
Podávanie tiazidových diuretík vrátane hydrochlorotiazidu s vitamínom D alebo s vápenatými soľami môže zosilniť zvýšenie sérového vápnika. Súbežné používanie tiazidových diuretík a vápenatých solí môže spôsobiť hyperkalciémiu u pacientov s predispozíciou na hyperkalciémiu (napr. Hyperparatyreóza, neoplazmy alebo stavy sprostredkované vitamínom D) zvýšením tubulárnej reabsorpcie vápnika.
Antidiabetické lieky (inzulín a perorálne antidiabetiká)
Tiazidové diuretiká môžu narušiť toleranciu glukózy. Možno bude potrebné upraviť dávku antidiabetických liekov.
Metformín sa má používať s opatrnosťou kvôli riziku laktátovej acidózy vyvolanej možným zlyhaním obličiek spojeným s hydrochlorotiazidom.
Beta -blokátory a diazoxid
Súbežné používanie tiazidových diuretík vrátane hydrochlorotiazidu a beta-blokátorov môže zvýšiť riziko hyperglykémie. Tiazidové diuretiká, vrátane hydrochlorotiazidu, môžu zvýšiť hyperglykemický účinok diazoxidu.
Lieky používané na liečbu dny (probenecid, sulfinpyrazon a alopurinol)
Možno bude potrebné upraviť dávku urikosurických liekov, pretože hydrochlorotiazid môže zvýšiť hladiny kyseliny močovej v sére. Možno bude potrebné zvýšiť dávku probenecidu alebo sulfinpyrazónu. Súbežné podávanie tiazidových diuretík vrátane hydrochlorotiazidu môže dávku zvýšiť. Výskyt reakcií z precitlivenosti na alopurinol.
Anticholinergiká a iné lieky ovplyvňujúce pohyblivosť žalúdka
Biologická dostupnosť diuretík tiazidového typu môže byť zvýšená anticholinergikami (napr. Atropín, biperiden), zrejme v dôsledku zníženia gastrointestinálnej motility a rýchlosti vyprázdňovania žalúdka.Naopak, predpokladá sa, že prokinetické lieky, ako je cisaprid, môžu znižovať biologickú dostupnosť tiazidových diuretík.
Amantadina
Tiazidy vrátane hydrochlorotiazidu môžu zvýšiť riziko nežiaducich reakcií spôsobených amantadínom.
Živice na výmenu iónov
Absorpciu tiazidových diuretík vrátane hydrochlorotiazidu znižuje cholestyramín alebo kolestipol. To môže mať za následok subterapeutické účinky tiazidových diuretík. Avšak distribúciou dávky hydrochlorotiazidu a živice tak, aby bol hydrochlorotiazid podávaný najmenej 4 hodiny pred alebo 4-6 hodín po podaní živíc, by interakcia mohla byť potenciálne minimalizovaná.
Cytotoxické činidlá
Tiazidy, vrátane hydrochlorotiazidu, môžu znížiť renálne vylučovanie cytotoxických liekov (napr. Cyklofosfamid, metotrexát) a zvýšiť ich myelosupresívne účinky.
Nedepolarizujúce relaxanty kostrového svalstva (napr. tubokurarín)
Tiazidy vrátane hydrochlorotiazidu zosilňujú účinok relaxancií kostrového svalstva, ako sú deriváty kurare.
Cyklosporín
Súbežné podávanie cyklosporínu môže zvýšiť riziko hyperurikémie a komplikácií dny.
Alkohol, barbituráty a omamné látky
Súbežné používanie tiazidových diuretík s inými látkami, ktoré majú tiež účinok znižujúci krvný tlak (napr. Látky, ktoré znižujú aktivitu sympatického centrálneho nervového systému alebo majú priamu vazodilatačnú aktivitu), môže zosilniť ortostatickú hypotenziu.
Metyldopa
Ojedinele boli hlásené prípady hemolytickej anémie vyskytujúcej sa pri súbežnom podávaní metyldopy a hydrochlorotiazidu.
Jódové kontrastné látky
V prípade dehydratácie vyvolanej diuretikami sa zvyšuje riziko akútneho zlyhania obličiek, najmä pri vysokých dávkach jodizovaných produktov. Pred podaním musia byť pacienti rehydratovaní.
04.6 Tehotenstvo a dojčenie -
Tehotenstvo
Valsartan
Použitie antagonistov receptora angiotenzínu II (AIIRA) sa neodporúča počas prvého trimestra gravidity (pozri časť 4.4). Použitie AIIRA je kontraindikované počas druhého a tretieho trimestra gravidity (pozri časti 4.3 a 4.4).
Epidemiologické dôkazy o riziku teratogenity po expozícii ACE inhibítorom počas prvého trimestra gravidity nie sú presvedčivé; malé zvýšenie rizika však nemožno vylúčiť. Aj keď nie sú k dispozícii žiadne kontrolované epidemiologické údaje o riziku s antagonistami receptorov angiotenzínu II (AIIRA), podobné riziko môže existovať aj pre túto triedu liekov. U pacientok plánujúcich graviditu sa má použiť alternatívna antihypertenzívna liečba. S preukázaným bezpečnostným profilom na použitie v tehotenstve, pokiaľ sa pokračovanie terapie AIIRA nepovažuje za nevyhnutné. Keď je diagnostikované tehotenstvo, liečba AIIRA sa má okamžite ukončiť a ak je to vhodné, má sa začať alternatívna liečba.
Je známe, že expozícia AIIRA počas druhého a tretieho trimestra indukuje u ľudí fetálnu toxicitu (znížená funkcia obličiek, oligohydramnión, spomalenie osifikácie lebky) a neonatálnu toxicitu (zlyhanie obličiek, hypotenzia, hyperkaliémia) (pozri tiež odsek 5.3).
Ak dôjde k expozícii AIIRA od druhého trimestra gravidity, odporúča sa ultrazvuková kontrola funkcie obličiek a lebky.
Novorodenci, ktorých matky užívali AIIRA, by mali byť starostlivo sledovaní kvôli hypotenzii (pozri časti 4.3 a 4.4).
Hydrochlorotiazid
Skúsenosti s používaním hydrochlorotiazidu počas gravidity, najmä v prvom trimestri, sú obmedzené. Štúdie na zvieratách sú nedostatočné. Hydrochlorotiazid prestupuje placentou. Na základe farmakologického mechanizmu účinku hydrochlorotiazidu môže jeho použitie počas druhého a tretieho trimestra gravidity zhoršiť perfúziu plodu a placenty a spôsobiť fetálne a neonatálne účinky, ako je žltačka, porucha elektrolytov a trombocytopénia.
Čas kŕmenia
Nie sú k dispozícii žiadne údaje o použití valsartanu počas laktácie. Hydrochlorotiazid sa vylučuje do materského mlieka. Preto sa používanie Combisartanu počas laktácie neodporúča. Na použitie počas laktácie by sa mala uprednostniť alternatívna terapia s preukázaným bezpečnostným profilom, obzvlášť pri dojčení novorodencov a dojčiat.
04.7 Účinky na schopnosť viesť vozidlá a obsluhovať stroje -
Neuskutočnili sa žiadne štúdie o účinku Combisartanu na schopnosť viesť vozidlá a obsluhovať stroje. Pri vedení vozidla alebo obsluhe strojov je potrebné vziať do úvahy možnosť príležitostných závratov alebo únavy.
04.8 Nežiaduce účinky -
Nežiaduce reakcie hlásené v klinických štúdiách a laboratórne nálezy, ktoré sa vyskytujú častejšie pri valsartane + hydrochlorotiazide ako pri placebe, a jednotlivé správy po uvedení lieku na trh sú uvedené nižšie podľa tried orgánových systémov. Nežiaduce reakcie známe pre každú jednotlivú zložku samotnú, ale nepozorované v klinických štúdiách, sa môžu vyskytnúť aj počas liečby valsartanom / hydrochlorotiazidom.
Nežiaduce reakcie sú zoradené podľa frekvencie, začínajúc od najčastejších, podľa nasledujúcej konvencie: veľmi časté (≥1 / 10); časté (≥ 1/100,
V rámci každej frekvenčnej triedy sú nežiaduce účinky hlásené zostupne podľa závažnosti.
Tabuľka 1. Frekvencia nežiaducich reakcií pri valsartane / hydrochlorotiazide
Získajte viac informácií o jednotlivých komponentoch
Nežiaduce reakcie už hlásené pre každú z jednotlivých zložiek môžu byť tiež potenciálnymi nežiaducimi účinkami Combisartanu, aj keď nie sú pozorované v klinických štúdiách alebo v období po uvedení lieku na trh.
Tabuľka 2. Frekvencia nežiaducich reakcií pri valsartane
Tabuľka 3. Frekvencia nežiaducich reakcií pri hydrochlorotiazide
Hydrochlorotiazid je už mnoho rokov široko predpisovaný, často vo vyšších dávkach, než aké sa podávajú s Combisartanom.U pacientov liečených ako monoterapia tiazidovými diuretikami vrátane hydrochlorotiazidu boli hlásené nasledujúce nežiaduce reakcie.
04.9 Predávkovanie -
Príznaky
Predávkovanie valsartanom môže mať za následok výraznú hypotenziu, ktorá môže viesť k zníženiu úrovne vedomia, obehovému kolapsu a / alebo šoku. Po predávkovaní hydrochlorotiazidom sa môžu vyskytnúť aj nasledujúce príznaky a symptómy: nauzea, somnolencia, hypovolémia, poruchy elektrolytov spojené so srdcovou arytmiou a svalovými kŕčmi.
Liečba
Terapeutické opatrenia závisia od času požitia a od typu a závažnosti symptómov, pričom sa uprednostňuje normalizácia obehových podmienok.
V prípade hypotenzie by mal byť pacient uložený na chrbte a rýchlo podaný fyziologický roztok.
Valsartan nemožno odstrániť hemodialýzou kvôli jeho silnej väzbe na plazmatické proteíny, zatiaľ čo hydrochlorotiazid je možné odstrániť dialýzou.
05.0 FARMAKOLOGICKÉ VLASTNOSTI -
05.1 "Farmakodynamické vlastnosti -
Farmakoterapeutická skupina: Antagonisty angiotenzínu II v kombinácii s diuretikami, valsartanom a diuretikami, ATC kód: C09D A03.
Valsartan / hydrochlorotiazid
V dvojito zaslepenej, randomizovanej, aktívne kontrolovanej štúdii u pacientov neadekvátne kontrolovaných 12,5 mg hydrochlorotiazidu bolo pozorované signifikantne väčšie zníženie systolického / diastolického krvného tlaku pri kombinácii valsartan / hydrochlorotiazid 160 / 12,5 mg. (12,4 / 7,5 mmHg) v porovnaní na hydrochlorotiazid 25 mg (5,6 / 2,1 mmHg). Okrem toho reagoval významne vyšší podiel pacientov (krvný tlak
V dvojito zaslepenej, randomizovanej, aktívne kontrolovanej štúdii u pacientov neadekvátne kontrolovaných 160 mg valsartanu sa pozorovali signifikantne väčšie poklesy systolického / diastolického krvného tlaku pri kombinácii valsartan / hydrochlorotiazid 160/25 mg (14,6 / 11,9 mmHg) a valsartan / hydrochlorotiazid 160 / 12,5 mg (12,4 / 10,4 mmHg) v porovnaní s valsartanom 160 mg (8,7 / 8,8 mmHg).
Štatistickú významnosť dosiahol aj rozdiel v znížení krvného tlaku medzi dávkami 160/25 mg a 160 / 12,5 mg. Okrem toho reagovalo výrazne vyššie percento pacientov (diastolický krvný tlak
V multifaktoriálnej, randomizovanej, dvojito zaslepenej štúdii porovnávajúcej rôzne dávky kombinácií valsartan / hydrochlorotiazid a príslušných zložiek boli pri kombinácii valsartan / hydrochlorotiazid 160 / 12,5 mg (17,8 / 13,5 mmHg) pozorované významne väčšie poklesy systolického / diastolického krvného tlaku. ) a 160/25 mg (22,5 / 15,3 mmHg) oproti placebu (1,9 / 4,1 mmHg) a ich príslušným monoterapiám, tj hydrochlorotiazid 12,5 mg (7,3 / 7,2 mmHg), hydrochlorotiazid 25 mg (12,7 / 9,3 mmHg) a valsartna 160 mg ( 12,1 / 9,4 mmHg). Okrem toho reagoval významne vyšší podiel pacientov (diastolický tlak
V kontrolovaných klinických skúšaniach s valsartanom + hydrochlorotiazidom došlo k zníženiu sérového draslíka v závislosti od dávky. Pokles draslíka v sére sa vyskytoval častejšie u pacientov, ktorí dostávali 25 mg hydrochlorotiazidu, ako u tých, ktorí dostávali 12,5 mg. V kontrolovaných klinických skúšaniach s valsartanom / hydrochlorotiazidom bol účinok hydrochlorotiazidu na zníženie draslíka oslabený účinkom valsartanu šetriaceho draslík.
Priaznivé účinky kombinácie valsartanu a hydrochlorotiazidu na kardiovaskulárnu mortalitu a morbiditu nie sú v súčasnosti známe.
Epidemiologické štúdie ukázali, že dlhodobá liečba hydrochlorotiazidom znižuje riziko kardiovaskulárnej mortality a morbidity.
Valsartan
Valsartan je perorálne aktívny špecifický antagonista receptora angiotenzínu II (Ang II). Selektívne pôsobí na podtyp receptora AT1, zodpovedný za známe účinky angiotenzínu II. Zvýšenie plazmatických hladín Ang II v dôsledku blokády receptorov AT1 valsartanom môže stimulovať neblokované receptory AT2, čo zrejme vyvažuje činnosť receptorov AT1. Valsartan nevykazuje žiadnu čiastočnú agonistickú aktivitu na receptore AT1 a má oveľa väčšiu (približne 20 000-násobnú) afinitu k receptoru AT1 ako k receptoru AT2. Valsartan sa neviaže na iné hormonálne receptory ani iónové kanály, ktoré sú známe svojou dôležitosťou v kardiovaskulárnej regulácii, a neblokuje ich.
Valsartan neinhibuje ACE, tiež známu ako kinináza II, ktorá prevádza Ang I na Ang II a degraduje bradykinín. Pretože neexistuje žiadny účinok na ACE alebo zosilnenie účinkov bradykinínu alebo látky P, antagonisty receptora angiotenzínu II nie sú pravdepodobne spojené s kašľom. V klinických štúdiách, kde bol valsartan porovnávaný s ACE inhibítorom, bol výskyt suchého kašľa významne (P
Podávanie valsartanu pacientom s arteriálnou hypertenziou vyvoláva zníženie krvného tlaku bez ovplyvnenia srdcovej frekvencie.
U väčšiny pacientov po podaní jednorazovej perorálnej dávky dôjde k nástupu antihypertenzného účinku do 2 hodín a maximálne zníženie krvného tlaku sa dosiahne do 4 až 6 hodín. Antihypertenzívny účinok pretrváva viac ako 24 hodín po podaní. Pri opakovanom podávaní s akoukoľvek dávkou sa maximálne zníženie krvného tlaku zvyčajne dosiahne do 2 až 4 týždňov a pretrváva počas dlhodobej liečby. Významné zníženie krvného tlaku sa získa spojením liečiva s hydrochlorotiazidom.
Náhle prerušenie valsartanu nebolo spojené s rebound hypertenziou alebo inými nežiaducimi klinickými udalosťami.
U pacientov s hypertenziou s diabetom 2. typu a mikroalbuminúriou bolo preukázané, že valsartan znižuje vylučovanie albumínu v moči. Štúdia MARVAL (zníženie albuminúrie albumínom s valsartanom) hodnotila zníženie vylučovania albumínu v moči (UAE) valsartanom (80-160 mg / od) vs. amlodipín (5-10 mg / od), u 332 pacientov s diabetom 2. typu (priemerný vek: 58 rokov; 265 mužov) s mikroalbuminúriou (valsartan: 58 mcg / min; amlodipín: 55,4 mcg / min), normálny alebo zvýšený krvný tlak a neporušená funkcia obličiek (kreatinín
V štúdii Diovan Reduction of Proteinuria (DROP) sa ďalej hodnotila účinnosť valsartanu pri znižovaní vylučovania albumínu v moči (UAE) u 391 hypertenzných pacientov (TK = 150/88 mmHg) s diabetom 2. typu, albuminúria (priemer = 102 mcg / min; 20 -700 mcg / min) a neporušenú funkciu obličiek (priemerný sérový kreatinín = 80 mcmol / l). Pacienti boli randomizovaní do jednej z troch rôznych dávok valsartanu (160, 320 a 640 mg / od) a boli liečení 30 týždňov. Cieľom tejto štúdie bolo stanoviť optimálnu dávku valsartanu na zníženie UAE u hypertenzných pacientov s diabetom typu 2. Po 30 týždňoch sa percentuálna zmena UAE významne znížila o 36% oproti východiskovým hodnotám. S valsartanom 160 mg (95% CI : 22% až 47%) a 44% s valsartanom 320 mg (95% IS: 31% až 54%). Zistilo sa, že 160-320 mg valsartanu spôsobuje klinicky významné zníženie UAE u hypertenzných pacientov s diabetom 2. typu.
Iné: duálna blokáda systému renín-angiotenzín-aldosterón
Dve veľké randomizované kontrolované štúdie (ONTARGET (ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) a VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) skúmali použitie kombinácie inhibítora ACE s antagonistom receptor angiotenzínu II.
ONTARGET bola štúdia vykonaná u pacientov s anamnézou kardiovaskulárneho alebo cerebrovaskulárneho ochorenia alebo diabetes mellitus 2. typu spojeného s dôkazom poškodenia orgánov.VA NEPHRON-D bola štúdia vykonaná u pacientov s diabetes mellitus 2. typu a diabetickou nefropatiou.
Tieto štúdie nepreukázali žiadny významný priaznivý vplyv na renálne a / alebo kardiovaskulárne výsledky a úmrtnosť, pričom v porovnaní s monoterapiou bolo pozorované zvýšené riziko hyperkaliémie, akútneho poškodenia obličiek a / alebo hypotenzie.
Tieto výsledky sú vzhľadom na ich podobné farmakodynamické vlastnosti relevantné aj pre iné inhibítory ACE a antagonisty receptora angiotenzínu II.
Inhibítory ACE a antagonisty receptora angiotenzínu II by sa preto nemali používať súčasne u pacientov s diabetickou nefropatiou.
ALTITUDE (Aliskiren Trial in Diabetes Type 2 Using Cardiovascular and Renal Disease Endpoints) bola štúdia zameraná na overenie výhody pridania aliskirenu k štandardnej terapii inhibítorom ACE alebo antagonistom receptora angiotenzínu II u pacientov s diabetes mellitus. Typu 2 a chronickým ochorením obličiek kardiovaskulárne ochorenie alebo oboje. Štúdia bola ukončená predčasne kvôli zvýšenému riziku nežiaducich udalostí. Kardiovaskulárna smrť a mozgová príhoda boli v skupine s aliskirenom numericky častejšie ako v skupine s placebom a nežiaduce udalosti a závažné nežiaduce udalosti, o ktoré je záujem ( hyperkaliémia, hypotenzia a renálna dysfunkcia) boli hlásené častejšie v skupine s aliskirenom ako v skupine s placebom.
Hydrochlorotiazid
Miesto účinku tiazidových diuretík je prevažne v distálnom stočenom tubule obličky. Prítomnosť vysokoafinitného receptora v obličkovej kôre sa ukázala ako primárne väzbové miesto pre účinok tiazidových diuretík a inhibíciu transportu. NaCl v distálnom stočenom tubule. Mechanizmus účinku tiazidov sa deje prostredníctvom inhibície transportu Na + Cl-, pravdepodobne konkurenciou s miestom Cl-, čím je ovplyvnený mechanizmus reabsorpcie elektrolytov: priame zvýšenie „vylučovania“ sodíka a chlóru v ekvivalentných množstvách a nepriamo znížiť objem plazmy týmto diuretickým pôsobením, s následným zvýšením plazmatickej renínovej aktivity, vylučovaním aldosterónu a stratou draslíka v moči a znížením sérového draslíka. Spojenie renín-aldosterón je sprostredkované angiotenzínom II, takže pri súčasnom podávaní valsartanu je pokles sérového draslíka menej výrazný ako ten, ktorý sa pozoruje pri monoterapii hydrochlorotiazidom.
05.2 "Farmakokinetické vlastnosti -
Valsartan / hydrochlorotiazid
Systémová dostupnosť hydrochlorotiazidu je pri súčasnom podávaní s valsartanom znížená približne o 30%. Kinetika valsartanu nie je súbežným podávaním s hydrochlorotiazidom významne ovplyvnená. Pozorovaná interakcia nemá vplyv na použitie valsartanu a hydrochlorotiazidu v kombinácii, keďže kontrolované klinické skúšania preukázali jasný antihypertenzívny účinok, lepší ako účinok dosiahnutý pri dvoch účinných látkach podávaných jednotlivo alebo pri placebe.
Valsartan
Absorpcia
Po perorálnom podaní sa maximálne koncentrácie valsartanu dosahujú po 2 až 4 hodinách. Jeho priemerná absolútna biologická dostupnosť je 23%. Jedlo znižuje expozíciu (meranú pomocou AUC, plocha pod krivkou plazmatickej koncentrácie) valsartanu o približne 40% a maximálnu plazmatickú koncentráciu (Cmax) o približne 50%, aj keď približne 8 hodín po podaní plazmatických koncentrácií valsartanu sú podobné na lačno aj nalačno. Toto zníženie AUC však nie je sprevádzané klinicky významným znížením terapeutického účinku, preto sa valsartan môže užívať s jedlom alebo bez jedla.
Distribúcia
Rovnovážny distribučný objem valsartanu po intravenóznom podaní je približne 17 litrov, čo naznačuje, že valsartan sa extenzívne nedistribuuje do tkanív. Valsartan sa vo veľkej miere (94-97%) viaže na sérové proteíny, predovšetkým na sérový albumín.
Biotransformácia
Valsartan nie je vo vysokej miere biotransformovaný, pretože iba asi 20% dávky sa izoluje ako metabolity. V plazme boli identifikované nízke koncentrácie hydroxylovaného metabolitu (menej ako 10% AUC valsartanu), ktorý je farmakologicky neaktívny.
Vylúčenie
Valsartan vykazuje multiexponenciálnu kinetiku rozpadu (t½α trus (približne 83% dávky) a moč (približne 13% dávky), predovšetkým ako nezmenené liečivo. Po intravenóznom podaní je plazmatický klírens približne 2 l / h. Jeho renálny klírens je 0,62 l / h (približne 30% celkového plazmatického klírensu). Polčas eliminácie valsartanu je 6 hodín.
Hydrochlorotiazid
Absorpcia
Po perorálnom podaní sa hydrochlorotiazid rýchlo absorbuje (tmax = približne 2 hodiny). V terapeutickom rozmedzí je priemerné zvýšenie AUC lineárne a úmerné dávke.
Vplyv jedla na absorpciu hydrochlorotiazidu, ak k nemu dôjde, má malý klinický význam. Absolútna biologická dostupnosť hydrochlorotiazidu po perorálnom podaní je 70%.
Distribúcia
Zdanlivý distribučný objem je 4-8 l / kg. Cirkulujúci hydrochlorotiazid sa viaže na sérové proteíny (40-70%), predovšetkým na sérový albumín. Hydrochlorotiazid sa tiež hromadí v erytrocytoch v množstvách približne 3 -krát vyšších ako plazmatické hladiny.
Vylúčenie
Hydrochlorotiazid sa eliminuje prevažne ako nemodifikovaná zlúčenina. V konečnej fáze eliminácie je hydrochlorotiazid eliminovaný z plazmy s priemerným polčasom v rozmedzí od 6 do 15 hodín. Kinetika hydrochlorotiazidu sa pri opakovanom podávaní dávky nemení a akumulácia je minimálna, keď Podáva sa jedenkrát denne. Viac ako 95% absorbovanej dávky hydrochlorotiazidu sa vylučuje v nezmenenej forme močom. Renálny klírens pozostáva z pasívnej filtrácie a aktívnej sekrécie v renálnom tubule.
Špeciálne populácie
Seniori
U niektorých starších osôb bola pozorovaná o niečo vyššia systémová expozícia valsartanu ako u mladých jedincov; nepreukázalo sa však, že by to malo klinický význam.
Obmedzené údaje naznačujú, že systémový klírens hydrochlorotiazidu je u zdravých aj hypertenzívnych starších ľudí v porovnaní s mladými zdravými dobrovoľníkmi znížený.
Porucha funkcie obličiek
Pri odporúčaných dávkach Combisartanu nie je potrebná úprava dávky u pacientov s rýchlosťou glomerulárnej filtrácie medzi 30 a 70 ml / min. Nie sú k dispozícii žiadne údaje o podávaní Combisartanu pacientom s ťažkým poškodením funkcie obličiek (rýchlosť glomerulárnej filtrácie a plazmatické bielkoviny sa neodstraňujú dialýzou, zatiaľ čo hydrochlorotiazid sa môže odstrániť dialýzou.
V prítomnosti poškodenia funkcie obličiek sa priemerné maximálne plazmatické hladiny a hodnoty AUC hydrochlorotiazidu zvyšujú a rýchlosť eliminácie močom klesá. U pacientov s miernym až stredne ťažkým poškodením funkcie obličiek sa pozorovalo 3-násobné zvýšenie AUC. U pacientov s ťažkou poruchou funkcie obličiek bolo pozorované 8-násobné zvýšenie AUC. Hydrochlorotiazid je kontraindikovaný u pacientov s ťažkou poruchou funkcie obličiek (pozri časť 4.3).
Poškodenie funkcie pečene
Vo farmakokinetickej štúdii vykonanej u pacientov s miernou (n = 6) alebo stredne ťažkou (n = 5) poruchou funkcie pečene sa expozícia valsartanu zvýšila približne 2-násobne v porovnaní so zdravými dobrovoľníkmi (pozri časti 4.2 a 4.4). Nie sú k dispozícii údaje o použití valsartanu u pacientov s ťažkou hepatálnou dysfunkciou (pozri časť 4.3). Ochorenie pečene nemá významný vplyv na farmakokinetiku hydrochlorotiazidu.
05.3 Predklinické údaje o bezpečnosti -
Potenciálna toxicita kombinácie valsartan / hydrochlorotiazid podávaná perorálne sa skúmala na potkanoch a opiciach (kosman) v štúdiách trvajúcich až 6 mesiacov. Neexistujú žiadne výsledky, ktoré by vylučovali použitie terapeutických dávok u ľudí.
V štúdiách chronickej toxicity boli asociáciou vyvolané zmeny s najväčšou pravdepodobnosťou spôsobené valsartanom. Toxikologicky zameraným orgánom boli obličky, s oveľa výraznejšou reakciou u opice ako u potkana. Táto kombinácia mala za následok poškodenie obličiek (nefropatia s tubulárnou bazofíliou, zvýšenie plazmatickej močoviny, kreatinínu v plazme a draslíka v sére, zvýšenie objemu moču a elektrolytov v moči od 30 mg / kg / deň valsartanu + 9 mg / kg / deň hydrochlorotiazidu u potkanov a 10 + 3 mg / kg / deň u opíc), pravdepodobne zmenou renálnej hemodynamiky. Tieto dávky u potkanov predstavujú 0,9 a 3,5 -násobok maximálnej odporúčanej dávky pre ľudí (MRHD) valsartanu a hydrochlorotiazidu v mg / m². U opíc tieto dávky predstavujú 0,3 a 1,2 -násobok maximálnej dávky odporúčanej pre ľudí (MRHD). valsartanu a hydrochlorotiazidu v mg / m² (výpočty predpokladajú perorálnu dávku valsartanu 320 mg / deň v kombinácii s 25 mg / deň hydrochlorotiazidu a 60 kg pacienta).
Vysoké dávky kombinácie valsartan / hydrochlorotiazid spôsobili zníženie indexov červených krviniek (počet erytrocytov, hemoglobín, hematokrit) zo 100 + 31 mg / kg / deň u potkanov a 30 + 9 mg / kg / deň u opíc. Tieto dávky u potkanov predstavujú 3,0 a 12 -násobok maximálnej odporúčanej dávky pre ľudí (MRHD) valsartanu a hydrochlorotiazidu v mg / m². U opíc predstavujú tieto dávky 0,9 a 3,5 -násobok maximálnej odporúčanej dávky pre ľudí (MRHD) valsartanu a hydrochlorotiazidu v mg / m² (výpočty predpokladajú perorálnu dávku valsartanu 320 mg / deň v kombinácii s 25 mg / deň hydrochlorotiazidu a 60 kg pacient).
U opíc bolo pozorované poškodenie žalúdočnej sliznice (od 30 + 9 mg / kg / deň). Táto kombinácia tiež viedla k hyperplázii aferentných arteriol v obličkách (600 + 188 mg / kg / deň u potkanov a 30 + 9 mg / kg / deň u opice). Tieto dávky u opice predstavujú 0,9, respektíve 3 5 -násobok maximálnej odporúčanej dávky valsartanu a hydrochlorotiazidu pre ľudí (MRHD) v mg / m². U potkanov tieto dávky predstavujú 18 a 73 -násobok maximálnej odporúčanej ľudskej dávky (MRHD) valsartanu a hydrochlorotiazidu v mg / m² (výpočty predpokladajú perorálnu dávku valsartanu 320 mg / deň v kombinácii s 25 mg / deň hydrochlorotiazidu a 60 kg pacienta).
Vyššie uvedené účinky sú zrejme spôsobené farmakologickým pôsobením vysokých dávok valsartanu (blokáda inhibície uvoľňovania renínu indukovanej angiotenzínom II so stimuláciou buniek produkujúcich renín) a vyskytujú sa aj pri inhibítoroch ACE. Zdá sa, že nie sú relevantné pre terapeutické účely. dávky valsartanu u ľudí.
Kombinácia valsartan + hydrochlorotiazid nebola testovaná na mutagenitu, chromozomálny rozklad alebo karcinogenézu, pretože nebola dokázaná žiadna interakcia medzi týmito dvoma látkami. Tieto testy však boli vykonávané oddelene s valsartanom a hydrochlorotiazidom a nepreukázali mutagenitu, chromozomálny rozklad ani karcinogenitu.
U potkanov v dôsledku toxických dávok valsartanu pre matky (600 mg / kg / deň) počas posledných dní gravidity a počas laktácie došlo k nižšej miere prežitia, nižšiemu prírastku hmotnosti a oneskorenému vývoju (odlúčenie chrupavky) a otvoreniu zvukovodu) v potomstvo (pozri časť 4.6). Tieto dávky u potkanov (600 mg / kg / deň) sú približne 18 -násobkom maximálnej odporúčanej dávky pre ľudí v mg / m² (výpočty predpokladajú perorálnu dávku 320 mg / deň pre pacienta s hmotnosťou 60 kg) .
Podobné výsledky boli pozorované pre valsartan / hydrochlorotiazid u potkanov a králikov. V štúdiách embryo-fetálneho vývoja (segment II) s valsartanom / hydrochlorotiazidom na potkanoch a králikoch nebol dokázaný teratogenicita, bola však pozorovaná fetotoxicita spojená s toxicitou pre matku.
06.0 FARMACEUTICKÉ INFORMÁCIE -
06.1 Pomocné látky -
Jadro tabletu:
Mikrokryštalická celulóza,
Koloidný oxid kremičitý bezvodý,
Krospovidón,
Stearan horečnatý
Povlak:
Hypromelóza,
Macrogol 8000,
Mastenec,
Červený oxid železitý (E 172),
Oxid titaničitý (E 171).
06.2 Nekompatibilita “-
Nie je to relevantné.
06.3 Obdobie platnosti “-
3 roky
06.4 Špeciálne opatrenia na uchovávanie -
Skladujte pri teplote nepresahujúcej 30 ° C.
Uchovávajte v pôvodnom obale na ochranu pred vlhkosťou.
06.5 Charakter vnútorného obalu a obsah balenia -
PVC / PE / PVDC / Al alebo PVC / PVDC / Al blistre
14, 28, 56, 98, v kalendárových baleniach, 280 filmom obalených tabliet
Deliteľné jednodávkové blistre z PVC / PE / PVDC / Al alebo PVC / PVDC / Al
56 x 1, 98 x 1, 280 x 1 filmom obalených tabliet.
Na trh nemusia byť uvedené všetky veľkosti balenia.
06.6 Pokyny na použitie a zaobchádzanie s liekom -
Žiadne špeciálne pokyny.
07.0 DRŽITEĽ „REGISTRÁCIE NA REGISTRÁCII“ -
A. Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi, 3 - Florencia
08.0 REGISTRAČNÉ ČÍSLO -
AIC č. 034134039 - 160 mg / 12,5 mg filmom obalené tablety, 14 tabliet v PVC / PE / PVDC / Al blistri
AIC č. 034134041 - 160 mg / 12,5 mg filmom obalené tablety, 28 tabliet v blistri PVC / PE / PVDC / Al AIC č. 034134054 - 160 mg / 12,5 mg filmom obalené tablety, 56 tabliet v PVC / PE / PVDC / Al blistri
AIC č. 034134066 - 160 mg / 12,5 mg filmom obalené tablety, 98 tabliet v PVC / PE / PVDC / Al blistri
AIC č. 034134078 - 160 mg / 12,5 mg filmom obalené tablety, 98 x 1 tableta v PVC / PE / PVDC / Al blistri
AIC č. 034134080 - 160 mg / 12,5 mg filmom obalené tablety, 280 (10x28) tabliet v PVC / PE / PVDC / Al blistri
AIC č. 034134092 - 160 mg / 12,5 mg filmom obalené tablety, 280 (20x14) tabliet v PVC / PE / PVDC / Al blistri
09.0 DÁTUM PRVEJ REGISTRÁCIE ALEBO OBNOVENIA REGISTRÁCIE -
Dátum prvej registrácie: 25. júla 2004
Dátum posledného obnovenia: 29. mája 2010
10.0 DÁTUM REVÍZIE TEXTU -
Jún 2015